Существует множество физических и химических свойств, которые позволяют группировать элементы в таблице Менделеева. Одним из таких свойств является число электронов на последнем слое. Данная характеристика нередко становится ключевым при определении классификации элементов в металлы и неметаллы.
Металлы - это элементы, обладающие металлическими свойствами: хорошей электропроводностью, гибкостью, блеском. Число электронов на последнем слое у металлов склонно увеличиваться по мере движения отлево к правому верхнему углу таблицы Менделеева. Возрастание количества электронов на последнем слое обусловлено увеличением количества энергетических уровней и облегчает передачу электронов между атомами металлов при образовании металлической связи.
С другой стороны, неметаллы - это элементы, обладающие неметаллическими свойствами: плохой электропроводностью, хрупкостью, отсутствием блеска. У неметаллов обычно 4 и более электронов на последнем слое. Это обеспечивает стабильность и полноту таких структур, как молекулы и кристаллы, и в свою очередь, препятствует протеканию электронного тока между атомами.
Что такое электроны?
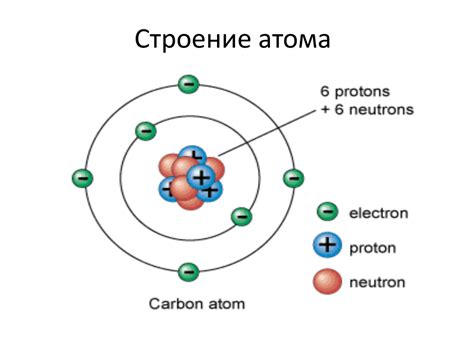
Электроны - это элементарные частицы, которые обладают отрицательным электрическим зарядом. Они являются одним из основных строительных блоков атомов и молекул, их поведение и взаимодействие играют важную роль во множестве физических и химических процессов.
Электроны находятся в постоянном движении вокруг ядра атома, заполняя энергетические уровни или оболочки. Последний энергетический уровень, на котором находятся электроны, называется внешней оболочкой. Количество электронов на внешней оболочке является важным фактором при определении химических свойств элемента.
Электроны могут переходить между энергетическими уровнями, поглощая или испуская энергию в виде фотонов. Этот процесс называется взаимодействием электронов с электромагнитным излучением и является основой для различных явлений, таких как свет и электричество.
Благодаря своим свойствам и способности к взаимодействию с другими элементами, электроны играют особую роль в химических реакциях. Они могут образовывать химические связи с другими атомами, обеспечивая разнообразие веществ и соединений.
Строение атома
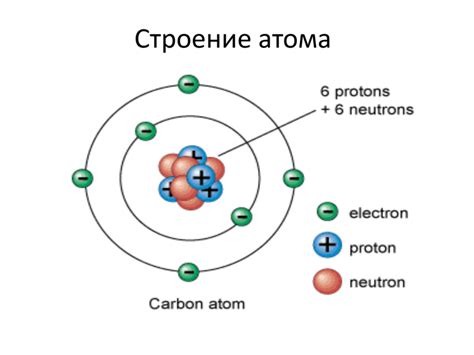
Атом – это основная единица химической структуры вещества. Он состоит из ядра, в котором находятся протоны и нейтроны, и облака электронов, движущихся по определенным энергетическим уровням или оболочкам.
Внешняя оболочка атома называется последним энергетическим уровнем или последней оболочкой. На этом уровне находятся электроны, которые принимают участие в химических реакциях и взаимодействуют с другими атомами.
Количество электронов на последнем энергетическом уровне определяет химические свойства атома и позволяет классифицировать его как металл или неметалл. Для металлов характерно наличие нескольких электронов на последнем уровне, что обусловлено их большим размером оболочек. Неметаллы же имеют 4 или более электрона на последней оболочке и обладают высокой электронной активностью.
Строение атома важно для понимания его химических свойств и реактивности. Знание числа электронов на последнем слое позволяет определить, каким образом атом будет взаимодействовать с другими атомами и формировать химические связи. Это помогает исследователям и химикам в создании новых веществ, а также в разработке новых материалов.
Металлы

Металлы - это класс веществ, обладающих характеристиками, такими как хорошая электропроводность и теплопроводность, упругость, пластичность и блеск. Они обычно имеют отличительную металлическую структуру, состоящую из регулярно расположенных атомов или ионов.
На последнем электронном слое у металлов обычно находятся от одного до трех электронов. Такое строение атомов обеспечивает их хорошую проводимость электричества и тепла. Электроны легко передвигаются по металлической структуре, что позволяет металлам быть отличными проводниками электричества и тепла.
Металлы имеют широкое применение в различных отраслях промышленности и строительства. Они используются для создания различных конструкций, инструментов, автомобилей, бытовой техники и многого другого. Также, металлы очень важны в электронике и электротехнике, благодаря своей электропроводности.
Некоторые известные металлы включают железо, алюминий, медь, свинец, золото и серебро. Каждый из этих металлов имеет свои уникальные свойства и применения. Например, железо используется для строительства и производства стали, алюминий - для изготовления легких и прочных конструкций, золото - для ювелирных изделий.
Число электронов на последнем слое у металлов
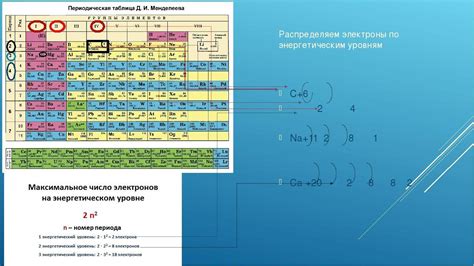
Металлы - это элементы, обладающие хорошей электропроводностью, благодаря свободно движущимся электронам в их структуре. Одной из важных характеристик металлов является число электронов на последнем слое.
Число электронов на последнем слое у металлов может варьироваться в зависимости от их положения в периодической таблице. Например, у щелочных металлов, таких как литий, натрий и калий, на последнем слое всего один электрон. Это объясняет их высокую реактивность и способность образовывать ионы с положительным зарядом.
Другие металлы, такие как магний, алюминий и железо, имеют два электрона на последнем слое. Это делает их более стабильными, чем щелочные металлы, и способными образовывать ионы со знаком +2.
Некоторые металлы, такие как железо, медь и цинк, имеют вариабельное число электронов на последнем слое. Например, железо может иметь два или три электрона на последнем слое, в зависимости от того, в какой степени окисления оно находится.
В общем, металлы имеют от одного до трех электронов на последнем слое. Это объясняет их способность проводить электричество и тепло, а также образовывать ионы с положительным зарядом.
Физические свойства металлов
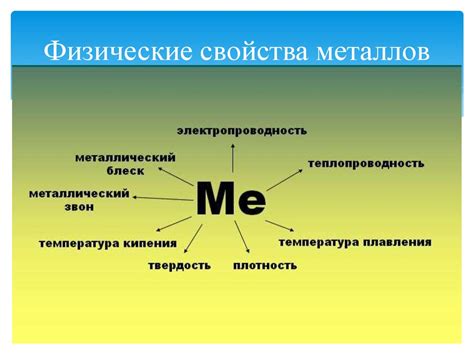
Проводимость электричества и тепла: Металлы обладают высокой проводимостью как электрического тока, так и тепла. Это объясняется наличием свободных электронов на внешнем энергетическом уровне. Именно они позволяют электронам легко перемещаться, обеспечивая электропроводность.
Пластичность и деформируемость: Одним из ключевых свойств металлов является их способность изменять форму под воздействием внешних сил. Благодаря особенностям кристаллической структуры и атомной решетки, металлы могут быть легко прокатаны, вытянуты и сжаты, не ломаясь.
Свечение и отражательная способность: Многие металлы обладают светящимся эффектом, который проявляется при нагревании или обработке. Это служит основой для создания различных источников света. Кроме того, металлы хорошо отражают свет и другие электромагнитные волны.
Высокая плотность: Металлы обычно обладают высокой плотностью, что означает, что в небольшом объеме содержится большое количество атомов. Использование металлов с высокой плотностью может быть полезно в различных отраслях, включая промышленность и строительство.
Магнитные свойства: Некоторые металлы проявляют магнитные свойства. Они могут притягиваться к магнитам или обладать способностью самостоятельно намагничиваться. Железо, никель и кобальт являются примерами магнитных металлов.
Неметаллы

Неметаллы - это элементы, которые обладают характеристиками, противоположными металлам. Они обычно имеют низкую плотность, низкую температуру плавления и кипения, а также слабую электропроводность. Неметаллы могут образовывать анионы, в основном путем приема электронов, чтобы достичь стабильной электронной оболочки.
Одной из главных характеристик неметаллов является то, что они имеют разную валентность - способность сформировать различное число химических связей. Это связано с количеством электронов на последнем энергетическом уровне. К примеру, кислород имеет 6 электронов на своем последнем энергетическом уровне, поэтому образует две ковалентные связи.
Неметаллы обладают различными химическими свойствами, их свойства зависят от их позиции в периодической системе. Например, кислород, азот и фтор являются газами при комнатной температуре, в то время как сера и фосфор - твердые вещества.
Интересно, что многие неметаллы являются важными компонентами в органической химии. Например, карбонаты и нитраты используются в качестве удобрений, этилен является основным компонентом в процессе обработки полимеров.
В целом, неметаллы играют важную роль во многих сферах нашей жизни, начиная от промышленности и науки до медицины и сельского хозяйства.
Число электронов на последнем слое у неметаллов
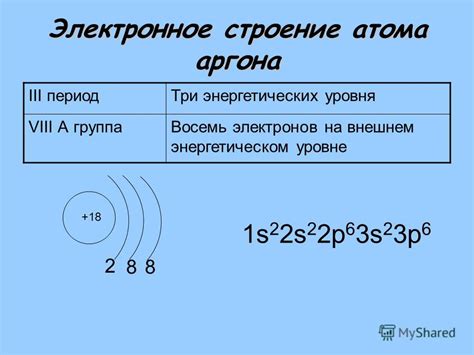
Неметаллы — это элементы, которые обладают относительно высокими значениями электроотрицательности. Это свойство влияет на их способность принимать или отдавать электроны в процессе химических реакций. Одной из характеристик неметаллов является количество электронов на последнем энергетическом слое.
Число электронов на последнем слое у неметаллов может быть разным и определяется порядковым номером элемента в таблице Менделеева. Например, у кислорода (O) на последнем слое находятся 6 электронов, у серы (S) — 6, у фтора (F) — 7, у хлора (Cl) — 7.
Подобная структура электронов обусловлена стремлением неметаллов заполнить свой последний энергетический слой полностью. Это позволяет им вступать в химические реакции с другими элементами и образовывать стабильные соединения.
Важным свойством неметаллов является способность притягивать электроны, что делает их хорошими окислителями при химических реакциях. У неметаллов, как правило, на последнем слое находится недостаточное количество электронов для полного заполнения. Это обуславливается их стремлением к стабильности и к полному шестиэлектронному октету.
В итоге, число электронов на последнем слое у неметаллов может варьироваться, но общая тенденция заключается в том, что неметаллы имеют от 4 до 7 электронов на последнем слое, что делает их активными реагентами и стремящимися к образованию стабильных соединений.
Физические свойства неметаллов

1. Электроотрицательность: Одной из основных характеристик неметаллов является их высокая электроотрицательность. Это означает, что неметаллы имеют большую способность притягивать к себе электроны в химических связях, что делает их крайне реактивными элементами.
2. Качественное состояние: Неметаллы чаще всего находятся в газообразном или жидком состоянии при комнатной температуре и атмосферном давлении. Некоторые неметаллы могут быть твердыми, но они обычно имеют низкую плотность и хрупкую структуру.
3. Электрическая проводимость: В отличие от металлов, неметаллы обычно являются плохими проводниками электричества. Они имеют высокое сопротивление электронному току, так как их электроны не свободно движутся по сравнению с металлическими элементами.
4. Теплопроводность: Неметаллы также обладают низкой теплопроводностью. Это означает, что они плохо проводят тепло и могут быть хорошими изоляторами тепла.
5. Окисление: Большинство неметаллов легко окисляются при контакте с кислородом из воздуха. Это может привести к образованию оксидов неметаллов, которые имеют различные свойства и могут быть использованы в различных химических реакциях.
6. Химическая активность: Неметаллы обычно являются очень активными химическими элементами. Они легко участвуют в химических реакциях и образуют различные соединения с другими элементами. Некоторые неметаллы могут быть ядовитыми или опасными для жизни.
Вопрос-ответ

Какое число электронов на последнем слое у металлов?
У металлов на последнем слое обычно находится одно или несколько электронов. Важно отметить, что число электронов на последнем слое может быть переменным в зависимости от конкретного металла.
Сколько электронов на последнем слое у неметаллов?
У неметаллов на последнем слое обычно находится от 4 до 8 электронов. Это связано с их стремлением заполнить свою внешнюю оболочку электронами, что делает их более реактивными и склонными к образованию химических связей.
