Цезий – элемент химической системы, обладающий свойствами и металлов, и неметаллов. Он находится в одной группе с другими щелочными металлами, такими как литий, натрий и калий. Однако, в отличие от своих соседей, цезий обладает свойствами неметалла в некоторых условиях.
На вид цезий – мягкий, серебристо-белый металл, который легко режется ножом. Он очень реактивен и может буриться при взаимодействии с воздухом, водой и органическими веществами. Эта химическая активность обусловлена присутствием одной внешней электронной оболочки, что делает его похожим на другие металлы.
Однако при достаточно высоких температурах цезий может проявлять свойства неметалла. В таких условиях он образует молекулярные соединения и проявляет кислотные свойства. Это объясняется тем, что при нагревании происходит разрыв металлической связи и электроны становятся несвязанными и перемещаются вокруг своих положительно заряженных ядер, образуя ионный кристалл.
Цезий: особенности химического элемента

Цезий – химический элемент периодической системы, которому присвоен символ Cs и атомный номер 55. Он относится к группе щелочных металлов и является одним из самых редких элементов в земной коре.
Цезий обладает рядом особенностей, которые делают его уникальным. Во-первых, цезий является мягким металлом с низкой плотностью, его плотность примерно в два раза меньше плотности воды. Это делает его очень легким и подвижным элементом.
Во-вторых, цезий имеет очень низкую температуру плавления – всего 28,5 градусов Цельсия. Это означает, что при комнатной температуре цезий находится в твердом состоянии, но при нагревании быстро переходит в жидкое состояние.
Кроме того, цезий обладает высокой химической активностью. Он реагирует с водой, воздухом и многими другими веществами. Из-за этой активности цезий в природе встречается в виде солей, в основном, в виде хлорида цезия.
Важным свойством цезия является его способность к горению. При соприкосновении с воздухом, цезий может воспламеняться, что делает его очень опасным для работы с ним. В прошлом цезий использовался для создания электронных устройств, но из-за высокой активности и опасности работы с ним, его использование стало ограниченным.
Таким образом, цезий – уникальный элемент с множеством особенностей. Его низкая плотность и температура плавления, химическая активность и способность к горению делают его интересным объектом изучения для ученых и неравнодушных к химии людей.
Цезий как химический элемент

Цезий (Cs) – химический элемент из группы щелочных металлов, обозначаемый символом Cs и имеющий атомный номер 55 в периодической таблице Менделеева. Он является одним из редких естественно встречающихся металлов и обладает рядом уникальных свойств.
Цезий имеет серебристо-белый цвет и мягкий, пластичный металлический блеск. Он очень реактивный металл и быстро окисляется на воздухе, образуя оксиды. Цезий также образует амиды, галогениды и множество солей, которые имеют важное применение в различных отраслях науки и техники.
Одной из уникальных химических особенностей цезия является его высокая реакционная способность с водой. При контакте с водой металл реагирует, образуя взрывоопасный газообразный цезийгидрид. Благодаря этой особенности цезий активно применяется в производстве полупроводниковых устройств, в качестве катализатора и в других химических процессах.
Цезий также обладает важными физическими свойствами. Он имеет низкую плотность и очень низкую температуру плавления, что делает его одним из самых легких металлов. Благодаря этим свойствам цезий широко применяется в производстве сплавов и в различных научных исследованиях.
Физические свойства цезия

Цезий – химический элемент, котоый относится к щелочным металлам. У него атомный номер 55 и химический символ Cs. Физические свойства цезия делают его уникальным элементом в таблице химических элементов.
Одной из особенностей цезия является его низкая плотность. Плотность цезия составляет около 1,93 г/см³, что делает его одним из самых легких металлов. Благодаря этому свойству, цезий легко плавится и испаряется при небольшой температуре. Точка плавления цезия составляет всего около 28,5°C, а точка кипения – около 678°C.
Цезий также известен своей мягкостью и пластичностью. Он является мягким металлом, который можно нарезать ножом. Более того, цезий имеет низкую твердость, позволяя легко формировать его в различные формы. Однако, из-за своей химической реактивности, цезий часто хранится в специальных контейнерах, чтобы предотвратить его окисление.
Цезий может быть также использован в электронике. Он имеет низкую работу выхода, что означает, что он может легко выделять электроны. Это свойство приводит к его широкому применению в фотоэлементах и других электронных устройствах. Кроме того, цезий имеет способность быть облучаемым ионами, что может быть использовано в процессе создания искусственных спутников Земли.
Химические свойства цезия
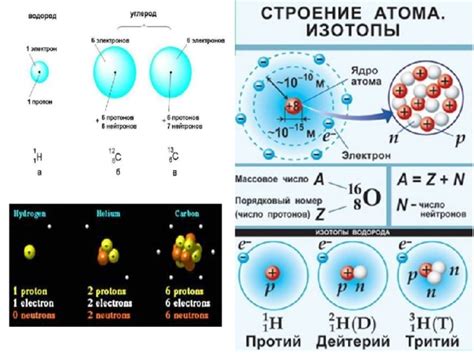
1. Электрохимические свойства: Цезий относится к активным металлам, он легко окисляется воздухом и реагирует с водой сообразно реакцией: 2Cs + 2H2O → 2CsOH + H2. Реакция цезия с кислородом приводит к образованию оксида цезия (Cs2O).
2. Химическая реакция с кислородом: Взаимодействие цезия с кислородом приводит к образованию цезия, диоксида (CsO2) - пищевое законодательство рекомендует этот продукт в качестве красителя. Также цезий образует ценные соли, например, перманганат цезия – насыщенный розовый окрашенный кристаллический порошок.
3. Химическое взаимодействие с водой: Цезий реагирует с водой, образуя щелочь цезия гидроксид (CsOH), который широко используется в производстве стекла и синтезе веществ. Это сильное основание, взаимодействует с кислотами сообразно типичным реакциям:
- 2CsOH + H2SO4 → Cs2SO4 + 2H2O
- 2CsOH + HCl → CsCl + H2O
- 2CsOH + HNO3 → CsNO3 + 2H2O
4. Гидриды: Цезий образует гидриды, например, цезийгидрид (CsH). Гидриды цезия широко применяются в производстве сплавов и полупроводниковых материалов.
5. Способность образовывать соединения с кислородом: Цезий способен образовывать соединения с кислородом, например, оксид цезия (Cs2O) и пероксид цезия (Cs2O2). Эти соединения используются в различных отраслях науки и промышленности.
6. Способность образовывать соединения с галогенами: Цезий образует соединения с галогенами, такие как цезийфторид (CsF), цезийхлорид (CsCl), цезийбромид (CsBr) и цезиййодид (CsI). Они широко применяются в фармацевтической и химической промышленности, а также в научных исследованиях.
Применение цезия в различных отраслях

1. Медицина. Цезий имеет применение в медицинской технологии, а именно в радиотерапии рака. Радиоактивный изотоп цезия-137 используется для лечения некоторых видов злокачественных опухолей. Это связано с его способностью уничтожать раковые клетки и останавливать их развитие.
2. Энергетика. Цезий играет важную роль в ядерной энергетике. Он используется в ядерных реакторах как подкладка для управляющих стержней, что позволяет контролировать реакцию деления атомов. Также цезий может использоваться для производства термоэлектрических преобразователей, которые преобразуют тепловую энергию в электрическую.
3. Электроника. Цезиевые соединения, такие как цезия-бромид, обладают полезными свойствами в электронике. Они используются в производстве фотоэлементов, катодов и детекторов гамма-излучения. Кроме того, цезиевые соединения могут применяться в процессе высокочастотного нагрева и вакуумной электронике.
4. Научные исследования. Изотоп цезия-133 является важным инструментом для научных исследований. Он используется в атомных часах, которые обеспечивают высокую точность времени. Атомные часы на основе цезия-133 в настоящее время используются в глобальных навигационных спутниковых системах, таких как GPS.
5. Производство стекла. Цезий окись (Cs2O) может использоваться в производстве стекла для получения специальных эффектов. Она придает стеклу особую прозрачность и светоотражающие свойства, что делает его привлекательным для производства оптических приборов и украшений.
6. Научный анализ. В аналитической химии цезий используется в качестве ионного маркера для идентификации определенных веществ и вещественных соединений. Он также может использоваться для калибровки аналитических приборов и улучшения точности их измерений.
Распространение цезия в природе и его значения
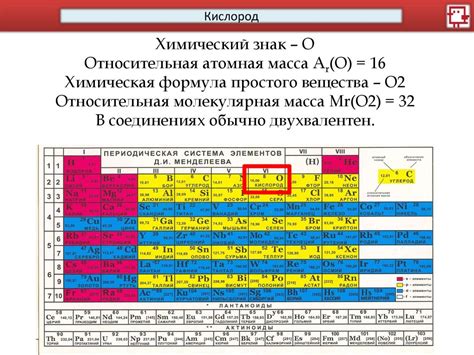
Цезий – химический элемент, обладающий металлическими свойствами, но при некоторых условиях проявляющий себя как полуметалл или неметалл. Основным источником цезия в природе является минерал петалит, который содержит около 3% данного элемента.
Хотя цезий встречается в природе в виде соединений, его редко можно обнаружить в свободном состоянии. В основном, разделяется в процессе добычи радиоактивных изотопов и в путевке при переработке ядерного топлива. Распределение цезия в природе достаточно широко, и его содержание часто связано с географическими особенностями территории. Так, в Южной Корее и Южной Америке его концентрация в почве может составлять около 10 микрограмм на 1 грамм, а в Калифорнии доходить до 100 микрограмм на 1 грамм.
Цезий играет важную роль в различных сферах применения, особенно в ядерной энергетике. Радиоактивный изотоп цезия-137 используется для медицинских и научных исследований, а также в промышленности и сельском хозяйстве. Однако надлежащая обработка и утилизация ядерных отходов, содержащих цезий, крайне важна для предотвращения загрязнения окружающей среды и здоровья людей.
Цезий также находит применение в электронике, особенно в разработке полупроводниковых приборов, в частности, в фотоэлементах. Некоторые соединения цезия используются в производстве стекла и эмалей, а также в производстве синтетических сапфировых кристаллов.
Вопрос-ответ

Цезий это металл или не металл?
Цезий является металлом. Он принадлежит к щелочным металлам и обладает химическим элементом Cs и атомным номером 55. В природе цезий встречается в виде минералов, но в основном получают его из минералов, богатых литием.
Какие свойства у цезия?
Цезий обладает следующими свойствами: он мягкий, серебристо-белый металл, имеет низкую плотность и плавится при относительно низкой температуре - около 28 градусов Цельсия. Цезий является очень реактивным веществом, легко окисляется воздухом и реагирует с водой, образуя гидроксид цезия и выделяя водород.
Для чего используют цезий?
Цезий имеет несколько применений. В первую очередь, его используют в научных исследованиях и атомных исследованиях. Кроме того, цезий может использоваться в электротехнике, особенно в функции вакуумных приборов, в термоэлектрических преобразователях и прочих устройствах. Еще одно важное применение цезия - в фоторецепторах на основе цезиевого селенида.
Какова опасность использования цезия?
Цезий и его соединения могут быть опасными для человека из-за их реактивности и токсичности. В частности, цезий-137 является радиоактивным изотопом и может представлять опасность для здоровья. Поэтому его использование должно быть строго контролируемым и подлежать специальным мерам безопасности.
