Железо – один из самых распространенных и важных элементов в периодической системе химических элементов. Оно широко применяется в различных отраслях промышленности, включая металлургию, строительство, энергетику и многие другие. Формирование цепочек по железу имеет огромное значение для понимания его химических свойств и возможностей применения.
Основные принципы образования цепочек по железу в химии связаны с его атомной структурой и способностью образовывать химические связи с другими атомами. Железо является переходным металлом и обладает большим количеством возможных окислительных состояний, что делает его химически активным и способным к реакциям с различными веществами.
Образование цепочек по железу может происходить через образование ковалентных или ионных связей. Ковалентная связь образуется при совместном использовании электронов внешней оболочки железа и атомов других элементов. Ионная связь, в свою очередь, образуется при передаче электронов от железа к другому атому или наоборот. Эти два механизма образования связей существенно влияют на химические и физические свойства цепочек по железу.
Принципы образования цепочек по железу в химии детально изучаются с помощью различных методов исследования, включая рентгеноструктурный анализ, спектроскопию и термические методы. Это позволяет установить структуру и компоненты цепочек, их стабильность и возможность использования в различных процессах.
Что такое цепочки по железу?

Цепочки по железу - это особый класс соединений, в которых железо играет ключевую роль в образовании связей. Железо может образовывать различные виды связей с другими элементами, такими как кислород, сера, углерод, азот и другие.
Цепочки по железу часто обладают особыми свойствами, что делает их интересными для изучения и применения в различных областях науки и технологий. Например, в биохимии цепочки по железу играют важную роль в процессах дыхания, транспорта кислорода и катализа реакций.
Одним из наиболее известных примеров цепочек по железу является гемоглобин, содержащий железо в своей структуре. Гемоглобин является основной составляющей красных кровяных клеток и отвечает за перенос кислорода от легких к тканям организма.
Помимо биологической роли, цепочки по железу также имеют широкое применение в различных отраслях химии и материаловедения. Например, железо играет важную роль в катализаторах, магнитных материалах, электронных устройствах и многом другом.
Определение понятия

Цепочка по железу - это последовательность химических реакций, в которых ион железа претерпевает изменения своей окислительной степени и переходит из одного состояния в другое. Железо может существовать в различных окислительных состояниях, таких как Fe2+ (железо со степенью окисления +2) и Fe3+ (железо со степенью окисления +3).
Цепочки по железу в химии играют важную роль, так как позволяют понять, как ионы железа участвуют в различных реакциях, и какие процессы происходят при их окислении и восстановлении. Это важно для понимания реакций окисления-восстановления, которые часто встречаются в органической и неорганической химии.
Цепочки по железу могут быть представлены в виде таблицы или списка реакций, где каждая реакция соответствует переходу железа из одного окислительного состояния в другое. Такая таблица позволяет систематизировать и изучать реакции окислительно-восстановительных процессов с участием железа.
Изучение цепочек по железу позволяет лучше понять химические свойства железа и его соединений, а также применять этот знания в различных областях, например, в медицине, при изготовлении оптических материалов и других материалов, а также в пищевой и фармацевтической промышленности.
Принцип образования цепочек

Принцип образования цепочек – одно из важных понятий в химии, которое связано с концепцией строения и связей в молекулах соединений. Он объясняет, как и почему атомы различных элементов объединяются в определенном порядке, образуя цепочки или скелеты молекул.
Основной принцип образования цепочек заключается в том, что атомы стремятся установить наиболее стабильные связи, чтобы достичь наименьшей энергии. В основе этого принципа лежит концепция электронного строения атомов, где образуются связи за счет обмена или совместного использования электронов валентной оболочки.
Различные элементы имеют разную валентность и способность образовывать связи с другими атомами. Эта способность зависит от количества электронов в валентной оболочке и стремления атомов достичь октета, то есть наличия в валентной оболочке 8 электронов.
Принцип образования цепочек применяется при анализе структуры и свойств органических соединений, таких как углеводороды, аминокислоты и другие органические молекулы. Он позволяет предсказывать форму и реакционную способность молекул на основе их структуры и атомных связей.
Взаимодействие элементов
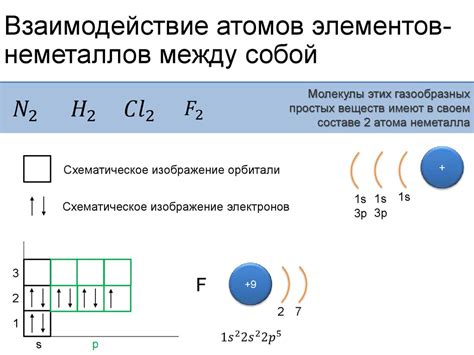
В химии элементы взаимодействуют друг с другом, образуя различные соединения. Взаимодействие элементов может происходить по разным принципам: обмен электронами, образование координационных соединений, а также образование ионных связей.
Один из способов взаимодействия элементов - обмен электронами. В этом случае один элемент отдает электроны, а другой элемент принимает их. При обмене электронами образуются новые соединения, в которых элементы связаны между собой.
Еще одним принципом взаимодействия элементов является образование координационных соединений. В этом случае один элемент (донор) отдает электроны другому элементу (акцептору), образуя комплекс. Координационные соединения часто образуются между металлами и не металлами.
Ионные связи - это еще один важный принцип взаимодействия элементов. При ионном связывании один элемент отдает электроны, становясь положительно заряженным ионом. Другой элемент принимает эти электроны, становясь отрицательно заряженным ионом. Причастные ионы связываются между собой на основе электростатического притяжения, образуя ионную сеть.
Таким образом, взаимодействие элементов играет ключевую роль в формировании различных соединений в химии. Обмен электронами, координационные соединения и ионные связи - это основные принципы, по которым элементы могут связываться и образовывать новые вещества.
Применение цепочек в химии

Цепочки в химии представляют собой последовательность связей между атомами, которые играют важную роль в определении физических и химических свойств веществ. Применение цепочек в химии помогает понять и предсказать реакционные свойства и структуру молекул.
Связь между атомами в химии является основой для формирования цепочек. Она может быть одиночной, двойной или тройной, и в зависимости от этого структура цепочки будет различной. Например, в молекуле этилена есть двойная связь между углеродными атомами, что делает ее плоской и позволяет проявиться делокализации электронной плотности.
Цепочки атомов образуют основу для образования различных органических и неорганических соединений. Через цепочки атомов можно описать строение комплексов, полимеров, органических соединений и многих других соединений, что позволяет затем предсказывать и объяснять их химические свойства.
Перечисление атомов в цепочке нередко осуществляется в виде нумерованного списка. Это удобно для анализа и сравнения различных цепочек, а также для обозначения позиций на них. Например, в молекуле пропана мы можем увидеть нумерацию углеродных атомов, что позволяет описать направление реакционной активности различных функциональных групп.
Кроме того, применение таблиц может существенно облегчить анализ и сравнение различных цепочек. Таблицы могут содержать информацию о длине и типе связей, атомах, функциональных группах и других свойствах цепочек. Такая организация данных помогает сделать систематизированный анализ и даёт возможность получить более полное представление о структуре и свойствах веществ.
Вопрос-ответ

Какие принципы лежат в основе образования цепочек по железу в химии?
Образование цепочек по железу в химии основано на нескольких принципах. Один из них - способность железа образовывать хелатные соединения со свободными лигандами. Железо может образовывать ковалентные связи с атомами других элементов, образуя цепочки. Также важным принципом является принцип охоты на свободные электроны, когда железо становится электрофильным и образует связи с электрон-донорами. Наконец, важной ролью играет и действие локальных зарядов, которые могут связывать железные атомы в цепочки.
Каким образом железо образует хелатные соединения?
Хелатные соединения создаются, когда железо образует ковалентные связи со свободными лигандами, обвивая их вокруг себя и образуя структуру, напоминающую клешню или зажим. Эти соединения обладают высокой стабильностью, в большей степени за счет особенностей электронного строения железа.
Какие факторы могут влиять на образование цепочек по железу?
Образование цепочек по железу может зависеть от нескольких факторов. Один из них - концентрация свободных лигандов. Чем больше свободных лигандов, тем больше возможностей для образования цепочек. Также важным фактором является электрофильность железа. Если железо обладает большим электрофильным потенциалом, то оно будет больше привлекать свободные электроны и образовывать цепочки.
Какое значение имеет образование цепочек по железу для химических процессов?
Образование цепочек по железу имеет важное значение для химических процессов. Это позволяет железу образовывать комплексы с другими соединениями и участвовать в различных реакциях. Такие цепочки могут служить катализаторами, активировать различные вещества или участвовать в электронном транспорте. Благодаря образованию цепочек, железо может выполнять разнообразные функции в химических процессах и играть важную роль в живых организмах.
