Кристаллические решетки металлов и ионные решетки являются двумя основными типами структур, которые обладают различными свойствами и основаны на различных взаимодействиях между атомами. Кристаллические решетки металлов являются примером сильно связанных решеток, в которых атомы расположены в упорядоченном повторяющемся порядке. Ионные решетки, с другой стороны, образуются за счет притяжения между положительными и отрицательными ионами и представляют собой более сложные структуры.
Одним из основных отличий между кристаллическими решетками металлов и ионными является тип связи между атомами. В кристаллических решетках металлов атомы образуют ковалентные или металлические связи, характеризующиеся обменом электронами между атомами. Это позволяет металлам обладать высокой электропроводностью и теплопроводностью, а также способностью быть деформированными без разрушения структуры.
Ионные решетки, напротив, состоят из положительных и отрицательных ионов, связанных притяжением электрических зарядов. Это приводит к высокой твердости и температуре плавления ионных соединений. Кроме того, ионные решетки обладают низкой электропроводностью, так как заряженные ионы не могут свободно передвигаться внутри решетки.
Структура кристаллических решеток металлов также отличается от структуры ионных решеток. В металлах атомы образуют трехмерные упорядоченные решетки, в то время как ионные соединения могут иметь различные типы структур, такие как кубическая гранецентрированная или гексагонально ближний упакованный.
Кристаллические решетки металлов и ионных соединений: различия и особенности
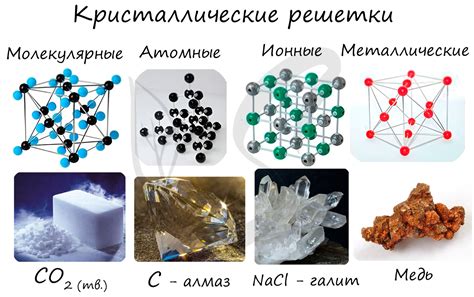
Металлы характеризуются кристаллической решеткой, которая образуется благодаря свободному движению электронов внутри материала. У металлов решетка состоит из положительно заряженных ионов, которые окружены общими электронами, образуя так называемое "море" электронов. Такая структура позволяет металлам быть хорошими проводниками тепла и электричества. Кристаллические решетки металлов обычно имеют простую геометрическую форму, например, кубическую, гексагональную или квадратную.
Ионные соединения, напротив, состоят из положительно и отрицательно заряженных ионов, которые образуют устойчивые кристаллические решетки. Уровень энергии таких соединений минимизируется благодаря сильным электростатическим взаимодействиям между зарядами ионов. Решетки ионных соединений обычно имеют сложную структуру, которую можно представить в виде трехмерной таблицы, содержащей положительные и отрицательные ионы, расположенные в определенном порядке. Ионные соединения обладают высокими температурными и точками плавления и обычно являются хрупкими.
Особенности кристаллических решеток металлов и ионных соединений обусловлены различными типами связей между атомами или ионами. В металлах связи между атомами осуществляются путем обмена свободными электронами, что позволяет им быть хорошими проводниками электричества. У ионных соединений, напротив, есть ярко выраженные положительные и отрицательные ионы, которые связываются электростатическими силами притяжения. Это обусловливает высокую плотность и твердость ионных соединений. Кроме того, такие соединения обладают четко определенными температурными и точками плавления и сохраняют свою устойчивость при высоких температурах.
Строение кристаллических решеток металлов
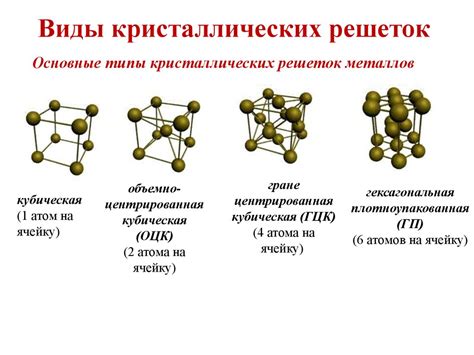
Металлы относятся к одному из классов кристаллических материалов. Их кристаллическая решетка характеризуется особыми свойствами, отличными от решетки ионных кристаллов.
В основе строения кристаллической решетки металлов лежит т.н. "металлическая связь". Это особый тип связи между атомами, который обуславливает их способность образовывать металлическую решетку. Основными характеристиками металлической связи являются деликатное равновесие между притяжением положительно заряженных атомных ядер и отталкиванием электронов, а также их свободное движение внутри решетки.
Структура кристаллической решетки металлов представляет собой регулярное повторение элементарной ячейки, которая состоит из атомов одного или нескольких элементов. Атомы в кристаллической решетке металлов располагаются в узлах кубической, гексагональной или иной периодической сетки. В результате этого образуется трехмерная сеть атомов, представляющая собой регулярное расположение атомов в пространстве.
Особенностью кристаллических решеток металлов является их высокая плотность. Металлические решетки обладают высокой симметрией и позволяют атомам занимать позиции с минимальной свободной энергией. Это делает металлы прочными и твердыми материалами с хорошей проводимостью тепла и электричества.
В целом, строение кристаллических решеток металлов отличается от ионных решеток своей спецификой, обуславливающей уникальные свойства металлов.
Строение ионных решеток: основные черты
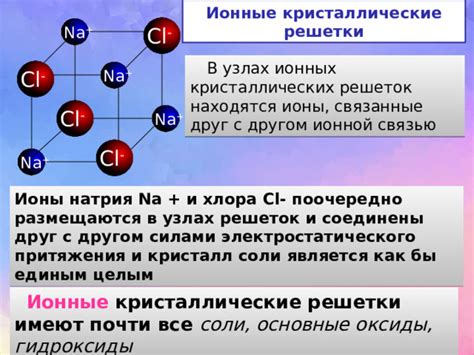
Ионные решетки являются особым типом кристаллической структуры, которая образуется при образовании ионных соединений. Они состоят из положительно и отрицательно заряженных ионов, которые располагаются в пространстве в определенном порядке.
Основными чертами ионных решеток являются регулярное расположение ионов в кристалле и наличие сильных электростатических взаимодействий между ними. Ионы могут быть разных размеров и иметь разные заряды, что влияет на структуру решетки и свойства соединения.
Структура ионной решетки определяется зарядом ионов и их радиусами. Положительно заряженные ионы называются катионами, а отрицательно заряженные - анионами. Катионы и анионы чередуются в решетке и образуют кристаллическую структуру.
В ионных решетках обычно присутствуют целеобразные отношения между катионами и анионами, которые обеспечивают электронейтральность соединения. При этом катионы и анионы могут между собой образовывать ионо-координированные связи, создавая стабильную структуру решетки.
Ионные решетки обладают рядом характеристических свойств, таких как высокая температура плавления, твердость, хрупкость и не проводимость электрического тока в твердом состоянии. Однако, в расплавленном или растворенном состоянии, ионные соединения могут проявлять электропроводность и обладать другими интересными свойствами.
Атомные составляющие металлических решеток

Металлические решетки состоят из атомов металла, которые образуют упорядоченное кристаллическое строение. Каждый атом металла окружен соседними атомами, образуя трехмерную сеть. Главными атомными составляющими металлических решеток являются атомы металла и свободные электроны.
Атомы металла в металлической решетке располагаются на регулярных интервалах иго известным порядком, что придает металлу его характерное кристаллическое строение и свойства. Атомы металла обычно имеют положительный заряд ядра и делят свои электроны с другими атомами металла. Этот обмен электронами придает металлицеским решеткам их особые электрические и теплопроводящие свойства.
Свободные электроны являются важной составляющей металлических решеток. Они образуют электронное облако, свободно перемещающееся в металле. Свободные электроны отвечают за электрическую проводимость металлов и их способность быть деформируемыми. Благодаря свободным электронам, металлы могут проводить электрический ток и иметь высокую теплопроводность.
Таким образом, атомы металла и свободные электроны представляют атомные составляющие металлических решеток. Эти компоненты обеспечивают металлам их особые физические свойства и характерные особенности кристаллической структуры.
Атомные составляющие ионных решеток

Ионные решетки состоят из атомных ионов, которые обладают положительным или отрицательным зарядом. Положительные ионы называют катионами, а отрицательные - анионами. Катионы и анионы располагаются в атомарных слоях, образуя упорядоченные структуры, называемые ионными решетками.
Катионы и анионы различаются по своей природе. Катионы обычно являются металлами, выделяются своей положительной зарядом и обладают хорошей проводимостью электричества. Анионы, в свою очередь, могут быть не только необходимыми элементами в определенных соединениях, но также могут иметь склонность к образованию кристаллических структур.
Важно отметить, что ионные решетки обладают высокой степенью упорядоченности. Атомы внутри ионных решеток занимают фиксированные позиции, образуя регулярные, повторяющиеся структуры. Катионы и анионы в ионных решетках находятся близко друг к другу и образуют сильные электростатические связи.
Атомные составляющие ионных решеток определяют их свойства. Например, структура ионной решетки влияет на ее механическую прочность, термическую стабильность и электропроводность. Различия в атомных составляющих могут приводить к различиям в химической активности ионных решеток, а также к их способности образовывать растворы или проводить электрический ток.
Уникальные свойства кристаллических решеток металлов
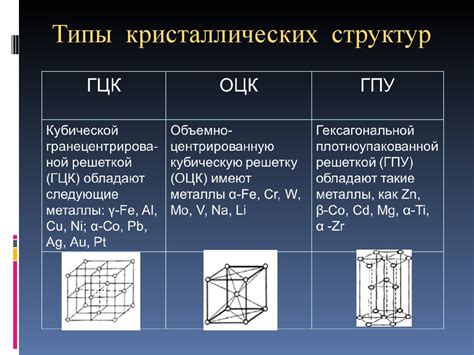
Кристаллические решетки металлов обладают рядом уникальных свойств, которые отличают их от ионных решеток. Одно из основных свойств металлических решеток - это высокая проводимость электричества и тепла. Благодаря свободным электронам, находящимся в металлической решетке, металлы могут эффективно проводить электрический ток и отдавать тепло. Это делает металлы основными материалами для проводников, генераторов электрической энергии и различных теплопереносных устройств.
Кроме того, кристаллические решетки металлов обладают высокой пластичностью и прочностью. Благодаря своей структуре, в которой атомы металлов могут смещаться без порождения дефектов, металлы могут легко подвергаться деформации и перекристаллизации. Это позволяет им быть устойчивыми к механическому напряжению и обладать высокой прочностью, что делает их применимыми в строительстве, авиации, автомобилестроении и многих других отраслях промышленности.
Металлические решетки также обладают способностью абсорбировать и отражать электромагнитные волны. Это свойство позволяет им быть использованными в производстве зеркал, антенн, солнечных панелей и других устройств, работающих на основе электромагнитного излучения. Кроме того, свободные электроны в металлических решетках способны разрушать связь между атомами газов, что делает металлы эффективными катализаторами химических реакций.
Особенности свойств ионных решеток
Ионные решетки представляют собой упорядоченные структуры, состоящие из положительно и отрицательно заряженных ионов. Эти решетки характеризуются рядом особенностей, влияющих на их свойства и связанные с этим явления.
Структура: Ионные решетки обладают регулярной и геометрически упорядоченной структурой, в которой положительные ионы (катионы) и отрицательные ионы (анионы) располагаются в определенном порядке. Это подтверждается наблюдением за формой кристаллов, которая характерна для ионных соединений.
Электростатические силы: Ионные решетки образуются благодаря силам электростатического притяжения между ионами разных зарядов. Эти силы обеспечивают прочное структурное соединение, поскольку они являются сильными и направленными.
Хрупкость: Ионные решетки обладают высокой хрупкостью, так как ионы в них занимают фиксированные позиции и не могут свободно перемещаться. Это свойство ионных решеток связано с их структурой и сопротивлением передвижению ионов по кристаллической решетке.
Проводимость: Ионные решетки являются слабо проводимыми электрическим током. Это связано с наличием связанных ионов в решетке, которые выступают в качестве преграды для свободного движения электронов.
Точка плавления: Ионные решетки имеют высокую точку плавления из-за прочного притяжения между ионами в кристаллической решетке. Данное свойство объясняет широкое применение ионных соединений в области высокотемпературных материалов и плавленого стекла.
Вопрос-ответ

Каковы основные отличия между кристаллическими решетками металлов и ионных соединений?
Основные отличия между кристаллическими решетками металлов и ионных соединений заключаются в строении и свойствах данных материалов. Кристаллические решетки металлов обладают металлической связью, где положительно заряженные ионы расположены в решетке регулярно и окружены облаком электронов, которые свободно движутся по решетке. Ионные соединения, в свою очередь, состоят из атомов с разными зарядами, которые образуют ионные связи между собой. В ионных соединениях, положительно и отрицательно заряженные ионы располагаются в решетке противоположных зарядов, образуя кристаллическую структуру. Также, металлы обладают хорошей электропроводностью и теплоотдачей, в то время как ионные соединения обычно являются непроводниками в твердом состоянии.
Каково строение кристаллических решеток металлов?
Кристаллические решетки металлов обладают особенным строением, которое называется металлической решеткой. В этой решетке положительно заряженные ионы металла расположены регулярно и окружены облаком свободных электронов, которые свободно движутся по всей решетке. Это объясняет характерную металлическую проводимость и теплоотдачу металлов. Кристаллические решетки металлов могут иметь различные формы в зависимости от типа металла и условий его кристаллизации. Примеры таких решеток включают кубическую, гексагональную и тетрагональную структуры.
