Строение атомов металлов и неметаллов отличается значительно друг от друга. Атомы металлов характеризуются высокой подвижностью электронов и отсутствием строгой границы между электронами внутренней оболочки и внешней электронной оболочкой. Благодаря этому металлы обладают высокой электропроводностью и теплопроводностью.
Строение атомов неметаллов отлично от строения атомов металлов. Неметаллы обладают несколькими внешними электронами, которые могут образовывать ковалентные связи с другими атомами. Данный тип связи обеспечивает высокую прочность межатомных связей и делает неметаллы хрупкими и легколетучими веществами.
Примером металлического атома может служить атом железа (Fe), который имеет 26 электронов. 2 электрона находятся во внешней электронной оболочке, и внутренняя оболочка может содержать до 18 электронов, что позволяет электронам свободно двигаться по атому и обеспечивает хорошую электропроводность.
В качестве примера атома неметалла можно рассмотреть атом кислорода (O), который имеет 8 электронов. Одинокий электрон во внешней оболочке хочет связаться с другим атомом, чтобы достичь стабильной восьмерочной конфигурации, и может образовать ковалентную связь.
Особенности строения атомов металлов и неметаллов определяют их химические, физические и электромагнитные свойства. Понимание этих особенностей имеет важное значение при изучении и применении различных материалов в инженерии, медицине и других отраслях науки и техники.
Строение атомов металлов и неметаллов:
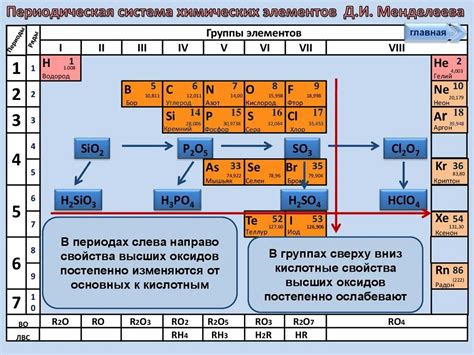
Атом является основным строительным блоком всех веществ, включая металлы и неметаллы. Атом металлов отличается от атомов неметаллов своим строением и свойствами.
Атомы металлов обычно имеют большой размер и низкую электронную плотность. Они имеют малое количество внутренних электронов, что делает их подвижными и хорошими проводниками электричества и тепла. Атомы металлов также обладают сильно положительно заряженными ядрами и большим количеством свободных электронов, которые могут перемещаться по решетке кристалла.
С другой стороны, атомы неметаллов имеют малый размер и высокую электронную плотность. Они обладают большим количеством внешних электронов, которые привлекаются к ядру сильно. Атомы неметаллов могут образовывать сильные ковалентные связи между собой, образуя молекулы или кластеры. Они плохо проводят электричество и тепло, так как электроны неметаллов плотно связаны с ядрами и не имеют свободной подвижности.
Особенности строения атомов металлов

Атомы металлов отличаются от атомов неметаллов своей структурой и свойствами. Одной из основных особенностей атомов металлов является наличие внешней электронной оболочки, содержащей малое количество электронов. В результате этого металлы обладают высокой проводимостью электричества.
Строение атомов металлов также связано с их металлической связью. Металлическая связь осуществляется между положительно заряженными ионами металлов и свободно движущимися электронами. Именно эта связь обуславливает способность металлов проводить электрический ток и тепло.
Кроме того, у атомов металлов присутствует свойство деформироваться под воздействием внешних сил. Это объясняется наличием свободных электронов в структуре атомов металлов, которые позволяют атомам смещаться относительно друг друга и образовывать металлическую решетку.
Примеры металлов с определенным строением атомов

Металлы характеризуются определенным строением своих атомов, что придает им уникальные свойства и своеобразные особенности. Рассмотрим несколько примеров металлов с определенными характеристиками строения атомов.
- Железо (Fe) - это металл с кубической решеткой гранецентрированного (ГЦК) типа. В данной структуре каждый атом железа окружен восемью атомами, расположенными в вершинах куба и одним атомом в центре каждой грани. Такое строение обуславливает высокую плотность и прочность железа.
- Алюминий (Al) - это металл с кубической решеткой гранецентрированного (ГЦК) типа, аналогичной решетке железа. Однако, структура алюминия отличается от железа тем, что первая имеет меньшую плотность и меньшую прочность.
- Магний (Mg) - это металл с гексагональной решеткой ближнего упорядочения (ГБУ). В данной структуре атомы магния располагаются в основном на плоскости и образуют шестиугольные ячейки. Такое строение делает магний легким и прочным металлом.
Таким образом, различные металлы имеют различное строение атомов, что напрямую влияет на их свойства и характеристики. Знание о строении атомов металлов позволяет более глубоко понять их поведение и использовать их в различных областях науки и промышленности.
Особенности строения атомов неметаллов
Атомы неметаллов обладают рядом особенностей, отличающих их от атомов металлов. Во-первых, неметаллы обычно обладают большим количеством электронов в своём внешнем энергетическом уровне. Это делает их более неподвижными и менее подверженными электрической проводимости.
Во-вторых, атомы неметаллов имеют более высокую электроотрицательность, что означает их большую способность притягивать электроны к своему ядру. В результате этого неметаллы обычно образуют ковалентные связи, где электроны между атомами распределяются равномерно.
Кроме того, атомы неметаллов могут составлять молекулы, объединяясь друг с другом с помощью ковалентных связей. Это позволяет неметаллам образовывать разнообразные структуры и соединения, включая полимеры и сетчатые материалы.
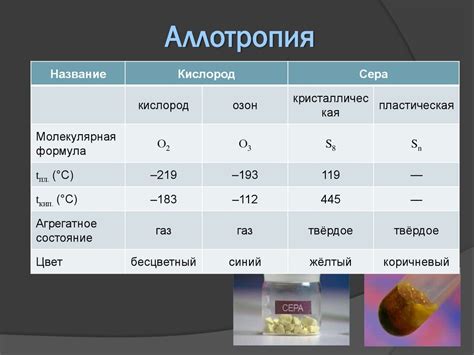
Некоторые примеры неметаллов включают кислород, азот, хлор, серу и фтор. Кислород, например, образует молекулы О2, которые являются основным компонентом воздуха и необходимы для поддержания жизни на Земле.
Таким образом, строение атомов неметаллов имеет свои уникальные особенности, которые определяют их химические и физические свойства. Понимание этих особенностей позволяет углубиться в изучение неметаллических элементов и их роли в мире химии и материаловедении.
Примеры неметаллов с определенным строением атомов

Кислород - один из основных неметаллов, который имеет атомную структуру с 8 электронами в валентной оболочке. Это делает его очень стабильным и реакционноспособным. Кислород представляет собой диатомный газ, то есть его молекула состоит из двух атомов, связанных парой электронов.
Фосфор также является неметаллом с определенным строением атомов. Каждый атом фосфора имеет 15 электронов, распределенных по разным энергетическим оболочкам. Валентная оболочка фосфора содержит 5 электронов, что делает его реакционноспособным элементом. Фосфор может формировать различные соединения, такие как фосфиды и оксиды.
Хлор - еще один пример неметалла с определенным строением атомов. Атом хлора содержит 17 электронов, из которых 7 находятся в валентной оболочке. Это делает хлор высоко реакционноспособным и хорошим окислителем. Хлор образует такие соединения, как хлориды, галогены и пероксиды.
Кроме того, некоторые неметаллы могут образовывать полимеры, такие как полиэтилен или полистирол. В этих полимерах молекулы неметаллов, таких как углерод и водород, связаны в длинные цепочки или сетки, что делает полимеры прочными и гибкими.
Все эти примеры неметаллов с определенным строением атомов и их химическими свойствами позволяют им играть важную роль в различных отраслях промышленности и науки, а также быть неотъемлемыми компонентами жизни на Земле.
Вопрос-ответ

Каково строение атомов металлов и неметаллов?
Строение атомов металлов и неметаллов различается. Атомы металлов обычно имеют большой размер и мало электронов в валентной оболочке. Они имеют металлическую структуру, где положительно заряженные ядра окружены облаком свободных электронов. Атомы неметаллов, напротив, имеют меньший размер и много электронов в валентной оболочке. Отличительной особенностью является то, что атомы неметаллов обычно образуют ковалентные связи, обмениваясь электронами с другими атомами, чтобы достичь стабильной конфигурации.
Какие примеры металлов существуют?
Металлы включают множество элементов, таких как железо, алюминий, медь, свинец, золото, серебро и т. д. Железо, например, является одним из самых распространенных металлов на Земле и используется во многих отраслях промышленности. Алюминий широко используется в производстве авиационных и автомобильных деталей, а также в строительной отрасли. Медь используется в электрических проводах и электронных устройствах из-за своей хорошей электропроводности и термической стабильности.
Какие примеры неметаллов существуют?
Неметаллы включают элементы, такие как углерод, кислород, азот, сера, фосфор и т. д. Углерод, например, является основным компонентом органических соединений и имеет разнообразные формы, такие как алмаз, графит и нанотрубки. Кислород является необходимым для дыхания и образует основу многих соединений, включая воду. Азот является ключевым компонентом в аминокислотах и белках. Сера используется в производстве удобрений и чистительных средств, а фосфор является необходимым элементом для роста растений и животных.
