Металлы и неметаллы - две основные категории химических элементов, которые имеют ряд различий между собой. Металлы обладают хорошей термической и электрической проводимостью, они способны отражать свет и обладают высокой пластичностью, что позволяет им изменять форму без разрушения. Неметаллы, напротив, характеризуются низкой электрической и теплопроводностью, они обычно являются непрозрачными и очень хрупкими.
Важным аспектом различия металлов и неметаллов является их химическая активность. Металлы обычно имеют большую склонность образовывать положительные ионы, тогда как неметаллы имеют склонность к образованию отрицательных ионов. Это является результатом различных электронных свойств элементов, в частности, их электроотрицательности.
Важно отметить, что металлы обычно обладают высоким плотностным состоянием и тяжелыми свойствами, в то время как неметаллы чаще имеют низкую плотность и легкие свойства. Металлы также имеют высокую температуру плавления и кипения, в то время как неметаллы имеют гораздо более низкие значения.
Сравнение металлов и неметаллов: в чем их отличия?

Металлы и неметаллы - это две основные группы элементов в таблице химических элементов. Они имеют различные физические и химические свойства, что делает их уникальными и самобытными. Рассмотрим их отличия по нескольким параметрам:
1. Проводимость электричества и тепла:
Металлы обладают высокой проводимостью электричества и тепла, в то время как неметаллы являются плохими проводниками электричества и тепла. Это связано с наличием свободных электронов в металлах, которые легко передвигаются по их структуре. Неметаллы же обладают коэвалентной связью, и электроны в их структуре не могут легко передвигаться.
2. Внешний вид и физические свойства:
Металлы обычно имеют блестящую поверхность и могут быть плавкими и деформируемыми. Они также обладают высокой плотностью, твердостью и точками плавления и кипения. Неметаллы, напротив, часто имеют матовую поверхность и являются хрупкими и негибкими. Они могут иметь низкую плотность и точку плавления и кипения.
3. Химические свойства и реактивность:
Металлы очень реактивны и, как правило, образуют положительные ионы. Они склонны терять электроны в химических реакциях и образовывать ионные связи с неметаллами. Неметаллы, наоборот, имеют тенденцию получать электроны в реакциях и образовывать ковалентные связи. Они могут образовывать отрицательные ионы и имеют различную степень электроотрицательности.
4. Использование в промышленности:
Металлы широко используются в промышленности для создания различных изделий, таких как автомобили, строительные материалы, инструменты и электрические провода. Неметаллы используются для производства пластмасс, стекла, удобрений и электронных компонентов.
В итоге, металлы и неметаллы имеют множество различий, начиная от их физических свойств до химической реактивности. Они играют важную роль в нашей повседневной жизни и промышленности, и их различия позволяют создавать разнообразные материалы и продукты.
Физические свойства

Металлы и неметаллы обладают различными физическими свойствами, которые отражают их особенности и способности. Одной из основных характеристик металлов является их высокая теплопроводность. Металлы способны передавать тепло эффективно благодаря свободному движению электронов в их структуре.
В отличие от металлов, неметаллы обычно имеют низкую теплопроводность. Они не обладают свободными электронами, способными передавать тепло, поэтому плохо проводят его через свою структуру. Это обуславливает использование металлов в различных инженерных и строительных приложениях, где требуется эффективная передача тепла.
Еще одной характеристикой металлов является их высокая плотность. Металлы обладают высокой массой при заданном объеме, что связано с наполнением их кристаллической решетки электронами. Именно благодаря высокой плотности металлы имеют крупнокристаллическую структуру и обладают высокой механической прочностью.
Неметаллы, в свою очередь, обычно имеют низкую плотность. Это связано с особенностями их атомной структуры и соединений. Различные неметаллы могут иметь различные плотности, но в целом они обычно легче металлов. Используя это свойство, неметаллы находят применение в производстве легких материалов, таких как пластик и резина.
Химическая активность
Химическая активность - важное свойство металлов и неметаллов, определяющее их способность вступать в химические реакции. Основным признаком химической активности является способность атомов вещества образовывать новые связи с другими атомами и ионами.
У металлов химическая активность высокая. Это связано с тем, что у них валентные электроны отделены от ядер и легко участвуют в реакциях. Металлы активно реагируют с кислородом, образуя оксиды, с водой, образуя гидроксиды, а также с кислотами, образуя соли.
Неметаллы, в отличие от металлов, имеют низкую химическую активность. Их валентные электроны плотно связаны с ядром и не участвуют в реакциях так активно, как валентные электроны металлов. Некоторые неметаллы могут вступать в реакции с металлами или другими неметаллами и образовывать соединения, но эти реакции происходят медленнее и менее интенсивно, чем реакции металлов.
Химическая активность металлов и неметаллов определяет их способности к образованию химических соединений и важна для понимания их роли в различных химических процессах и реакциях.
Проводимость электричества

Металлы: Металлы обладают высокой проводимостью электричества. Это связано с наличием свободных электронов в их структуре. Электроны могут свободно двигаться между атомами, создавая электрический ток. Кристаллическая структура металлов способствует легкому перемещению электронов. Это делает металлы отличными проводниками электричества.
Неметаллы: В отличие от металлов, неметаллы обычно не обладают высокой проводимостью электричества. У неметаллов внешняя электронная оболочка полностью заполнена электронами или частично заполнена их недостаточно для создания свободного электрического тока. Однако некоторые неметаллы, такие как графит, способны проявлять проводимость в определенных условиях.
Сравнение: Основное отличие между металлами и неметаллами в проводимости электричества связано с наличием или отсутствием свободных электронов. Металлы, благодаря свободным электронам, обладают высокой проводимостью, в то время как неметаллы, чаще всего, не способны проводить электрический ток. Это свойство металлов делает их необходимыми материалами для создания проводов и электрических контактов, а неметаллы используются в электронике и полупроводниковой промышленности в качестве изоляционных материалов.
Теплопроводность
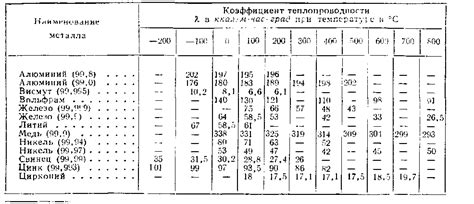
Теплопроводность является одним из основных различий между металлами и неметаллами. Металлы обладают высокой теплопроводностью, что означает, что они способны легко и быстро передавать тепло от одной части вещества ко всему объему. Неметаллы, напротив, имеют низкую теплопроводность, что означает, что они плохо проводят тепло и медленно передают его.
Причина этого различия заключается в структуре атомов веществ. В металлах атомы располагаются в регулярном кристаллическом решетке, что способствует быстрому передаче энергии. Неметаллы, наоборот, имеют сложную и неупорядоченную структуру, которая затрудняет передачу тепла.
Также, металлы часто содержат свободные электроны, которые могут свободно перемещаться и проводить тепло. Это дополнительно усиливает теплопроводность металлов. Неметаллы, напротив, не имеют свободных электронов и поэтому не способны эффективно проводить тепло.
Разница в теплопроводности между металлами и неметаллами имеет важное практическое значение. Из-за своей высокой теплопроводности, металлы широко используются в производстве теплообменных систем, теплопроводящих материалов и других устройствах, где важна эффективная передача тепла. Неметаллы, такие как пластик и древесина, обладают низкой теплопроводностью и часто используются для изоляции от тепла.
Плотность
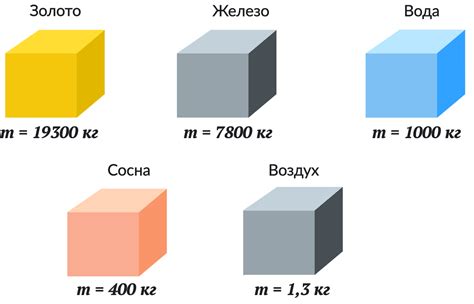
Плотность – это физическая характеристика вещества, указывающая на его массу в единицу объема. В контексте сравнения металлов и неметаллов, плотность является одним из основных критериев, которые отличают эти две группы элементов.
Металлы: В общем случае, металлы имеют высокую плотность. Например, элементы такие, как железо и свинец, обладают плотностью выше средней для этой группы. Однако, следует отметить, что плотность металлов может варьироваться в зависимости от конкретного элемента. Например, литий имеет низкую плотность, в то время как платина – высокую.
Неметаллы: В отличие от металлов, неметаллы обычно обладают низкой плотностью. Например, кислород и азот имеют низкую плотность. Однако, алмаз, являющийся формой углерода, может быть исключением из этого правила, так как он имеет высокую плотность.
Таким образом, плотность является одним из свойств, которое помогает различать металлы и неметаллы. В общем случае, металлы характеризуются высокой плотностью, тогда как неметаллы имеют низкую плотность. Однако, следует отметить, что данное свойство может варьироваться в зависимости от конкретного элемента.
Твердость и пластичность
Одним из главных различий между металлами и неметаллами является их твердость. Металлы обладают высокой твердостью, что означает, что они трудно поддаются деформации или исчерпанию. Неметаллы, напротив, обычно обладают низкой твердостью и легко поддаются деформации.
Металлы также обладают хорошей пластичностью, что означает, что они могут быть легко формованы и изменены без разрушения. Одновременно многие неметаллы, такие как стекло или керамика, обладают хрупкостью и могут легко разрушиться при деформации.
Твердость и пластичность металлов обусловлены их молекулярной структурой. Металлы обычно образуют кристаллическую решетку с регулярно упорядоченными атомами, что делает их твердыми и пластичными. Неметаллы, с другой стороны, образуют неупорядоченные структуры, что приводит к их хрупкости и низкой твердости.
- Примеры металлов с высокой твердостью и пластичностью: железо, алюминий, медь.
- Примеры неметаллов с низкой твердостью и хрупкостью: стекло, керамика, сера.
Твердость и пластичность являются важными свойствами материалов, которые определяют их возможности использования. Металлы, благодаря своей твердости и пластичности, широко используются в промышленности для изготовления различных изделий и конструкций. Неметаллы, хотя и обладают низкой твердостью, находят свое применение в производстве стекла, керамики и других хрупких материалов.
Оксиды и кислоты
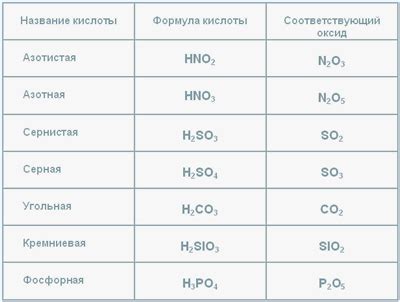
В химии существует два основных типа соединений, называемых оксидами и кислотами. Оксиды представляют собой химические соединения, в которых металл соединен с кислородом. Они обычно обладают щелочными свойствами и способны растворяться в воде, образуя щелочные растворы. Некоторые примеры оксидов включают оксид натрия, оксид алюминия и оксид железа.
Кислоты, с другой стороны, представляют собой соединения, в которых водород соединен с неметаллом. Они обычно обладают кислотными свойствами и могут реагировать с основаниями, образуя соль и воду. Некоторые примеры кислот включают серную кислоту, соляную кислоту и уксусную кислоту.
Оксиды и кислоты обладают различными свойствами и применениями. Оксиды широко используются в производстве стекла, керамики и металлургии. Они также могут использоваться в производстве удобрений и катализаторов. Кислоты, с другой стороны, имеют широкое применение в химической промышленности, медицине и пищевой промышленности.
Важно отметить, что некоторые соединения могут быть одновременно и оксидами, и кислотами. Например, оксид углерода (CO) может образовывать угольную кислоту (H2CO3), которая является слабой кислотой.
В общем, оксиды и кислоты представляют собой различные классы химических соединений с разными свойствами и применениями. Изучение этих соединений помогает нам более полно понять их химические и физические свойства, а также применение в различных отраслях промышленности.
Распространение в природе
Металлы являются широко распространенными элементами в природе. Многие металлы, такие как железо, алюминий и медь, встречаются в виде руд, которые могут быть добыты и обработаны для получения чистого металла. Руды обычно находятся в земле или горных породах и могут быть добыты путем различных методов, таких как шахтное дело и открытые разработки. После добычи руды проходит через процесс обогащения и переработки, чтобы из нее получить металлы высокой чистоты, которые могут использоваться в различных областях.
Неметаллы, в отличие от металлов, не обладают положительным зарядом и имеют химические свойства, противоположные металлам. Они обычно находятся в природе в виде газов, жидкостей или твердых веществ. Например, кислород - это один из наиболее распространенных неметаллов в природе и составляет около 21% атмосферного воздуха. Другие примеры неметаллов включают углерод, азот, серу и фосфор.
Некоторые неметаллы, такие как уголь и нефть, также используются в качестве источников энергии. Они являются основными компонентами природных ресурсов и используются для производства различных продуктов, таких как пластик, удобрения и лекарства. Некоторые неметаллы могут быть также использованы в промышленности для производства стекла, керамики и различных химических соединений.
Таким образом, металлы и неметаллы имеют разное распространение в природе. Металлы встречаются в виде руд, которые могут быть добыты и обработаны для получения чистого металла, в то время как неметаллы обычно находятся в природе в виде газов, жидкостей или твердых веществ.
Вопрос-ответ

Чем отличаются металлы от неметаллов?
Металлы и неметаллы отличаются в своих химических и физических свойствах. Металлы обладают хорошей теплопроводностью и электропроводностью, высокой плотностью и точкой плавления, а также отдают электроны и образуют положительно заряженные ионы. Неметаллы, напротив, обладают плохой теплопроводностью и электропроводностью, образуют отрицательно заряженные ионы и имеют низкую плотность и точку плавления.
В чем различия в химических свойствах металлов и неметаллов?
Металлы обычно образуют катионы, переносящие положительный заряд, в химических реакциях. Они обычно обладают высокой реакционной способностью и могут активно реагировать с другими веществами. Неметаллы, напротив, образуют анионы, переносящие отрицательный заряд. Они могут быть менее реакционноспособными и обычно образуют соединения с металлами, чтобы достичь стабильности.
