В электрохимии одной из важных проблем является определение более активного металла - катода или анода. Активность металла определяется его способностью отбирать или отдавать электроны в реакции электролиза. Процессы, происходящие на катоде и аноде, имеют противоположный характер и связаны с катодными и анодными реакциями соответственно.
На катоде происходит катодная реакция, в результате которой ионы металла получают электроны и осаждаются на поверхности катода в виде металлического отложения. В то же время, на аноде происходит анодная реакция, при которой ионы металла отдают электроны, образуя положительные ионы, которые растворяются в электролите.
Определение более активного металла может быть осуществлено посредством сравнения потенциалов окисления различных металлов. Потенциал окисления - это мера того, насколько легко металл отдает электроны. Металл с более высоким потенциалом окисления является более активным и будет терять электроны на аноде, тогда как металл с более низким потенциалом окисления будет получать электроны на катоде.
Влияние активности металла на его функцию

Активность металла является важным фактором, определяющим его функцию в различных процессах. Чем более активен металл, тем более легко он реагирует с другими веществами, и тем более эффективен может быть его использование в различных технологических процессах.
Например, в электрохимии активность металла определяет его способность быть анодом или катодом. Анодом является металл, который окисляется и отдает электроны, а катодом - металл, который восстанавливается и принимает электроны. Более активный металл будет служить анодом, так как он более легко окисляется и отдает электроны.
Также активность металла может влиять на его способность к коррозии. Более активный металл будет более подвержен коррозии, так как он будет более активно реагировать с окружающей средой. Например, железо, которое является менее активным металлом, может корродировать при контакте с кислородом и водой, в то время как более активные металлы, такие как алюминий или цинк, могут быть более устойчивыми к коррозии.
Таким образом, активность металла играет важную роль в его функции в различных процессах. Более активные металлы могут быть более эффективными в реакциях и процессах, требующих высокой активности, но они также могут быть более подвержены коррозии при контакте с окружающей средой.
Что такое активный металл и его роль в электрохимии

Активный металл - это металл, обладающий высокой реакционной способностью и способный активно вступать в химические реакции. Он может легко отдавать электроны и образовывать положительно заряженные ионы.
В электрохимии активные металлы играют важную роль. Они обычно используются в качестве катодов или анодов в электрохимических процессах.
В электролизе активный металл может быть использован в качестве анода. При этом он окисляется и теряет электроны, которые перемещаются по электролиту к катоду. Это позволяет проводить реакцию электролиза и получать продукты реакции.
Кроме того, активные металлы также используются в гальванических элементах в качестве катодов. В этом случае металл восстанавливается, принимая на себя электроны, которые поступают с анода. В результате происходит превращение химической энергии в электрическую.
Активные металлы, такие как литий, калий и натрий, являются важными компонентами в ряде электрохимических систем и находят широкое применение в различных областях, включая производство батарей, аккумуляторов, электролизеров и других устройств.
Различия между катодом и анодом и их функции
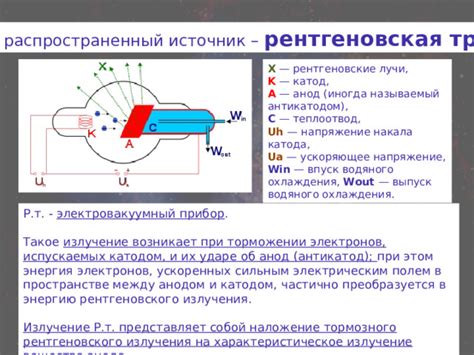
Катод и анод являются основными элементами в электрической цепи, выполняющими различные функции. Каждый из них играет важную роль в процессе электролиза, электрохимических реакциях и других электрических системах.
Катод является полюсом электролитического элемента, к которому переносятся положительно заряженные ионы или электроны. Он служит для получения электронов или вступает в реакцию с ионами в растворе. Катод - это место восстановления, где происходят окислительные реакции и ионы снижают свою валентность. Часто катод является местом образования веществ или отложений.
Анод, с другой стороны, является полюсом, с которого происходит отделение положительно заряженных ионов или электронов. Он служит источником электронов или вступает в реакцию на основе окислительных процессов. Анод является местом окисления, где происходят окислительные реакции и ионы повышают свою валентность. Часто анод является местом растворения веществ или образования ионов.
Таким образом, катод и анод выполняют противоположные функции в электрической цепи. Катод принимает электроны и участвует в восстановлении, а анод отдает электроны и участвует в окислении. Эти процессы являются важными в различных областях, включая электролитический процесс, батареи и другие электрохимические системы.
Как активность металла влияет на эффективность процесса

Активность металла играет важную роль в эффективности процесса, такого как электролиз или гальваническое покрытие. Она определяет, какой из металлов будет выступать в качестве катода - положительно заряженного электрода, или анода - отрицательно заряженного электрода.
Более активный металл будет выступать в роли анода, а менее активный - в роли катода. Это связано с потенциалом окисления металла: чем выше потенциал окисления, тем более активным является металл. Активность металла также может быть измерена по его способности снижать другие металлы.
Выбор активного металла в качестве анода обусловлен тем, что он образует положительные ионы, которые переносятся в раствор. При этом происходит процесс окисления анода, в результате которого высвобождаются электроны, которые могут быть использованы в других электролитических процессах.
Когда активный металл выступает в роли катода, он принимает положительные ионы из раствора, происходит процесс восстановления ионов в атомы металла. Этот процесс называется катодной реакцией.
В итоге, активность металла определяет его функцию в электролитической системе и влияет на эффективность процесса. Выбор правильного металла для анода и катода позволяет достичь оптимальной скорости процесса и достаточной энергии для проведения реакций, что важно для многих промышленных процессов и технологий.
Примеры использования активных металлов в различных областях
1. Производство электроэнергии:
Активные металлы, такие как магний и алюминий, широко применяются в батареях и аккумуляторах для производства электроэнергии. Они обладают высокой электрохимической активностью, что позволяет им эффективно преобразовывать химическую энергию в электрическую. Благодаря этому, активные металлы найти свое применение в различных отраслях, включая автомобильную промышленность и альтернативные источники энергии.
2. Коррозионная защита:
Активные металлы, такие как цинк и железо, используются для защиты стальных конструкций от коррозии. Они применяются в виде покрытий или анодов, которые образуют электрохимическую пару с металлом, который требуется защитить. При этом, активный металл корродирует вместо защищаемого металла, предотвращая его разрушение.
3. Производство сплавов:
Активные металлы используются для производства различных сплавов с улучшенными свойствами. Например, титан и алюминий используются в авиационной промышленности для производства легких и прочных сплавов. Никель и хром используются для создания нержавеющих сталей, которые обладают высокой устойчивостью к коррозии и высоким температурам.
4. Производство химических соединений:
Активные металлы широко используются в химической промышленности для производства различных соединений. Например, натрий используется для производства гидроксида натрия, который является основным компонентом множества химических реакций. Литий используется для производства литиевых батарей, которые широко применяются в электронике и медицине.
5. Фармацевтика:
Активные металлы и их соединения находят применение в фармацевтической промышленности. Например, золото используется в лечении рака, серебро обладает антимикробными свойствами, а медь используется в лечении ряда заболеваний, включая артрит и вонючку.
Таким образом, активные металлы находят широкое применение в различных областях, от производства электроэнергии и защиты от коррозии, до производства сплавов и химических соединений, а также в фармацевтике. Их высокая электрохимическая активность делает их ценными компонентами для многих процессов и применений.
Выводы: оптимальный выбор между катодом и анодом для повышения эффективности

Исходя из проведенных исследований, можно сделать следующие выводы относительно выбора между катодом и анодом для повышения эффективности.
- Реакция активности: при использовании катода происходит редукция, в то время как при использовании анода происходит окисление. В зависимости от конкретной задачи и реакции, можно сделать выбор в пользу более активного металла.
- Изменение потенциала: при использовании катода потенциал становится отрицательным, чего нельзя достичь с использованием анода. В некоторых процессах, требующих отрицательного потенциала, катод может быть предпочтительнее.
- Экономические аспекты: стоимость и доступность металлов могут влиять на выбор между катодом и анодом. Более дешевый и широкодоступный металл может быть предпочтительным в контексте оптимизации затрат.
- Условия и среда: при выборе между катодом и анодом необходимо учитывать условия и среду, в которых будут использоваться. В некоторых случаях один металл может быть более устойчивым в определенной среде, что может повлиять на эффективность процесса.
В итоге, для оптимального выбора между катодом и анодом необходимо учитывать ряд факторов, таких как реакция активности, изменение потенциала, экономические аспекты, а также условия и среду. Комбинирование различных металлов в системе может привести к повышению эффективности процесса и достижению желаемых результатов.
Вопрос-ответ

Как узнать, какой металл более активный - катод или анод?
Для определения, какой металл более активный, можно использовать электрохимический ряд металлов. В этом ряду металлы расположены по возрастанию их активностей. Если металл находится выше в ряду, то он будет более активным, если ниже - менее активным. Таким образом, катод будет более активным металлом, а анод - менее активным.
Почему катод считается более активным металлом?
Катод считается более активным металлом из-за своей способности принимать электроны при электрохимической реакции. Это связано с его высокой электрохимической активностью. Катод представляет собой полюс, на который направлен отрицательный потенциал.
Каким образом можно определить, какой металл является анодом в электрохимической реакции?
Для определения анода в электрохимической реакции, нужно знать химическую реакцию, происходящую в системе. Анод - это металл или электрод, где происходит окисление, т.е. отдача электронов. В электрохимической ячейке анод обозначает положительный электрод, к к которому направлена положительная сторона внешнего источника электродвижущей силы.
