Металлы – это элементы химической системы, которые обладают особыми свойствами. Одним из ключевых характеристик металлов является их способность образовывать ионные соединения, а именно, кратко удерживать внешние электроны.
По традиционной модели атома, электроны обращаются по орбитам вокруг ядра. Внешние электроны находятся на самой дальней от ядра орбите и называются валентными электронами. У атомов металлов количество валентных электронов отличается от других элементов, что делает их особенно устойчивыми и наиболее активными химическими веществами.
Металлы обладают маленьким радиусом атомов, что обеспечивает высокую электроотрицательность. Это значит, что атомы металлов сильно тянут на себя электроны и легко образуют ионные связи с другими элементами. Внешние электроны атомов металлов могут легко передаваться другим атомам или ионам. Это способствует образованию ионных соединений металлов, таких как соли или окислы.
Краткое удержание внешних электронов в атомах металлов позволяет им обладать рядом полезных свойств. Они обладают высокой теплопроводностью и электропроводностью, а также могут быть хорошими катализаторами. Большинство металлов обладают блестящей поверхностью, что делает их привлекательными для использования в ювелирных изделиях и других декоративных целях.
В целом, краткое удержание внешних электронов является одним из ключевых факторов, которые делают атомы металлов особенными и полезными в различных отраслях промышленности и науки.
Что такое атомы металлов и как они удерживают внешние электроны?

Атомы металлов представляют собой элементы периодической таблицы, которые характеризуются тем, что у них внешнее электронное облако содержит от одного до трех электронов. Эти электроны называются внешними или валентными электронами. Валентные электроны играют важную роль в химических свойствах металлов и определяют их способность образовывать соединения с другими элементами.
Удержание внешних электронов в атоме металла обеспечивается силой притяжения между ядром атома и электронами. В атоме металлов валентные электроны находятся на наибольшем энергетическом уровне, который называется валентной оболочкой. Эти электроны слабо связаны с ядром и могут легко участвовать в химических реакциях.
Атомы металлов имеют свободные структурные места в своей валентной оболочке, которые могут быть заняты внешними электронами от других атомов. Это позволяет атомам металлов образовывать кристаллическую решётку или металлические связи, при которых электроны свободно перемещаются между атомами.
Такая структура облегчает прохождение электрического тока через металлы и придает им высокую термическую и электрическую проводимости. Весьма интересно, что эти свойства атомов металлов можно объяснить их внутренней структурой и способностью к удержанию внешних электронов.
Понятие атомов металлов
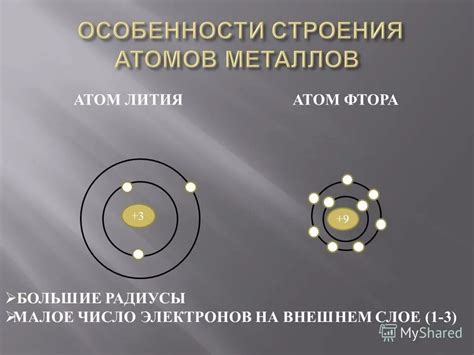
Атомы металлов являются основной единицей строения металлических материалов. Они обладают уникальными свойствами и играют важную роль в химической и физической природе металлов.
Атом металла состоит из ядра, которое содержит протоны и нейтроны, и облака электронов, которые обращаются вокруг ядра на определенных энергетических уровнях. Внешние электроны атома металла играют ключевую роль в его химических и физических свойствах.
Металлические атомы отличаются от атомов неметаллов тем, что они имеют мало валентных электронов в своей внешней оболочке. В связи с этим, металлы имеют способность образовывать ионные связи и проявлять свойства металлической проводимости, термической и электрической проводимости.
Кристаллическая решетка металла образуется благодаря упорядоченному расположению атомов, что создает характерные металлические структуры. В металлах атомы обычно находятся достаточно близко друг к другу, что обеспечивает их возможность обмена электронами и образования электрических связей.
Атомы металлов имеют свободные электроны, которые можно представить как «море электронов». Они могут свободно двигаться по металлической решетке и создавать электронное облако, которое обеспечивает высокую электропроводность металлов и их способность отражать свет.
Удержание внешних электронов атомами металлов
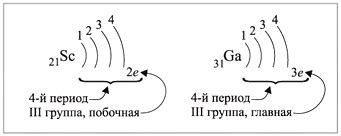
Внешние электроны атомов металлов, такие как натрий, калий или железо, играют важную роль в их химической активности. Они находятся на самом внешнем энергетическом уровне атома, так называемой валентной оболочке. Удержание этих внешних электронов атомами металлов обусловлено их внутренней структурой и свойствами.
Металлы обладают малым электроотрицательностью, что означает, что они имеют тенденцию отдавать свои внешние электроны другим атомам, образуя ионы положительного заряда. Это происходит из-за того, что у атомов металлов обычно недостаточно внешних электронов для заполнения своей валентной оболочки до заполнения. Поэтому они стремятся снизить свою энергию путем отдачи этих электронов.
Удержание внешних электронов также связано с энергетическими состояниями атома металла. Атомы металлов имеют низкую энергию, что позволяет им легко удерживать свои внешние электроны. Эта низкая энергия связана с внутренней структурой атома и его положением в периодической системе элементов.
Одна из основных особенностей удержания внешних электронов атомами металлов заключается в их способности образовывать металлические связи. При этом валентные электроны металла образуют общую «море» свободных электронов, которые легко двигаются по всему металлическому кристаллу. Это обеспечивает хорошую электропроводность и теплопроводность металлов.
Таким образом, удержание внешних электронов атомами металлов обусловлено их низкой электроотрицательностью, низкой энергией атома и способностью образовывать металлические связи. Все эти факторы определяют химические и физические свойства металлов и их способность взаимодействовать с другими веществами.
Вопрос-ответ

Что такое атомы металлов?
Атомы металлов - это атомы химического элемента, принадлежащего к классу металлов в периодической системе элементов.
Что такое внешние электроны атомов металлов?
Внешние электроны атомов металлов - это электроны, находящиеся на самых высокоэнергетических оболочках атомов металлов, то есть на оболочке, которая ближе всего к внешней оболочке атома.
Почему атомы металлов имеют краткое удержание внешних электронов?
Причина краткого удержания внешних электронов атомами металлов заключается в особенностях их электронной структуры. Внешние электроны в атомах металлов находятся на высокоэнергетических оболочках и слабо притягиваются к ядру атома. Из-за этого они легко удаляются и могут образовывать ион свободно двигающихся электронов в металле.
Какие элементы относятся к классу металлов?
К классу металлов относятся такие элементы, как натрий (Na), магний (Mg), алюминий (Al), железо (Fe), медь (Cu), цинк (Zn) и многие другие. Металлы обладают характерными свойствами: блеском, хорошей проводимостью тепла и электричества, пластичностью и т.д.
