Атомный вес металла – один из основных показателей, характеризующих химические свойства элемента. Этот параметр определяет массу атома металла в отношении к массе одного атома углерода-12, принятой за 12 единиц. Таким образом, атомный вес металла позволяет сравнивать элементы по их относительной массе и выявлять закономерности в их химическом поведении.
Важность атомного веса металла заключается в том, что он является основой для определения молекулярной массы соединений, в которых данный металл участвует. Зная атомный вес элемента и его количество в молекуле соединения, можно вычислить молекулярную массу и, соответственно, прогнозировать физические и химические свойства данного соединения.
Кроме того, атомный вес металла играет существенную роль в металлургической и полупроводниковой промышленности. Он определяет физические и механические свойства металлических материалов, таких как прочность, пластичность, электропроводность и теплопроводность. Более того, атомный вес металла связан с его распределением по периодической системе элементов и влияет на его возможные соединения и способы получения с помощью различных химических реакций.
Что такое атомный вес металла?

Атомный вес металла - это физическая величина, которая показывает массу одного атома данного металла. Она выражается в атомных единицах (у). Атомный вес металла можно найти в периодической системе химических элементов, где он указывается под именем элемента.
Атомный вес металла зависит от числа протонов и нейтронов в ядре атома. Также этот показатель может изменяться в зависимости от изотопов металла. Изотопы - это атомы, которые отличаются числом нейтронов в ядре.
Знание атомного веса металла имеет важное значение для различных научных и технических расчетов. Оно позволяет определить массовую долю каждого элемента в соединении или сплаве, а также провести различные расчеты, связанные с химическими реакциями и фазовыми переходами.
Атомный вес металла является ключевым показателем при работе с металлами, так как масса атома напрямую влияет на его свойства и химическую реактивность. Чем больше атомный вес металла, тем тяжелее и плотнее он будет иметь структуру, а также выше будет его температура плавления и кипения.
Определение атомного веса металла
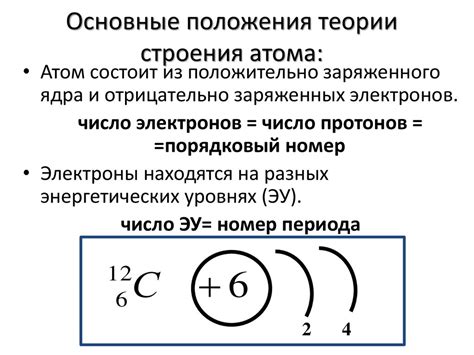
Атомный вес металла - это физическая величина, которая характеризует среднюю массу атомов данного металла, выраженную в атомных единицах (а.е.м.). Он позволяет сравнивать массу одного атома металла с массой других атомов.
Определение атомного веса металла включает в себя учет всех изотопов металла и их относительных содержаний в природе. Изотопы - это атомы элемента с одинаковым количеством протонов, но разным количеством нейтронов в ядре.
Для определения атомного веса металла используется таблица Менделеева, где указаны атомные массы всех элементов. Атомные массы приведены относительно массы атома углерода-12, которую приняли за 12 а.е.м. Таким образом, указанная в таблице атомная масса элемента означает, что масса его атома в несколько раз больше массы атома углерода-12.
Зная атомный вес металла, можно вычислить массу образца данного металла, а также проводить различные расчеты, связанные с его химическими и физическими свойствами. Атомный вес является важным параметром при проведении множества лабораторных работ и научных исследований в области металлургии, физики и химии металлов.
Молекулярный вес металла против атомного веса
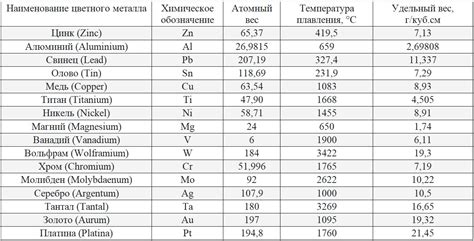
Молекулярный вес металла и атомный вес - две разные характеристики, связанные с химическими свойствами и структурой металлических веществ. Молекулярный вес показывает среднюю массу молекулы, состоящей из нескольких атомов металла, в то время как атомный вес указывает на массу одного атома данного металла.
Молекулярный вес металла определяется путем сложения масс всех атомов, входящих в его молекулу, и выражается в г/моль. Эта характеристика важна при проведении химических реакций и расчетах, так как она позволяет определить количество металла, необходимого для достижения определенного результата. Например, при подсчете стехиометрических соотношений реакций молекулярный вес металла является основным параметром.
С другой стороны, атомный вес металла является показателем массы отдельного атома данного металла и также выражается в г/моль. Он служит для определения количества атомов определенного металла в химической системе. Атомный вес используется для вычисления электрохимических свойств металлов, таких как атомный радиус, ионизационная энергия, атомный объем и т. д.
Итак, молекулярный вес металла и атомный вес взаимосвязаны, но имеют разные функции. Первый позволяет определить количество металла, необходимого для химических реакций и расчетов, в то время как второй является ключевым показателем для расчетов электрохимических свойств металлов.
Атомный вес металла и его значение
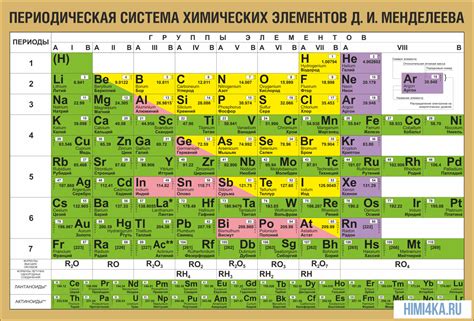
Атомный вес металла - это масса атома данного металла, выраженная в атомных единицах. Он играет важную роль в химии и материаловедении, так как влияет на свойства металла, его структуру и поведение в различных реакциях.
Атомный вес металла зависит от его атомного номера, т.е. числа протонов в ядре атома. Чем выше атомный номер металла, тем больше его атомный вес. Например, у металлов в периодической системе Менделеева атомный вес варьируется от нескольких граммов до нескольких сотен граммов на моль.
Атомный вес металла оказывает влияние на его физические и химические свойства. Чем выше атомный вес, тем выше плотность металла и его температура плавления. Также, атомный вес металла определяет его реакционную способность, скорость реакций и способность образовывать различные соединения.
Знание атомного веса металла позволяет ученым выбирать и оптимизировать материалы для различных применений. Например, основываясь на атомном весе металла, можно выбрать материал для изготовления конструкций, которые должны быть прочными и легкими одновременно.
Таким образом, атомный вес металла является важным параметром, определяющим его свойства и применение. Изучение атомного веса металлов позволяет лучше понять и контролировать их химические и физические свойства.
Как измеряется атомный вес металла?
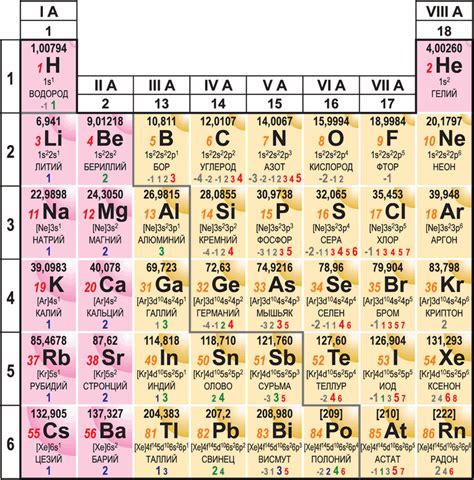
Атомный вес металла - это масса одного атома данного элемента, выраженная в атомных единицах. Измерить атомный вес металла можно с помощью различных методов и техник.
Один из таких методов - это масс-спектрометрия. В этом методе атомный вес металла определяется путем ионизации атомов металла и измерения массы ионов в масс-спектрометре. Такой подход позволяет получить точные данные об атомном весе металла.
Другим методом измерения атомного веса металла является использование химических реакций. Например, при известном количестве металла и реагента можно определить соотношение между их массами и вычислить атомный вес металла.
Также существует метод нейтронной активации, который основан на использовании реакции ядерного синтеза. Путем облучения металла нейтронами можно получить активированные ядерные изотопы и измерить их радиоактивность, что позволяет рассчитать атомный вес металла.
Все эти методы и техники позволяют определить атомный вес металла с высокой точностью, что важно для многих научных и промышленных исследований.
Формула атомного веса металла

Атомный вес металла – это средний вес атома данного металла относительно веса атома углерода-12.
Формула для расчета атомного веса металла имеет следующий вид:
Атомный вес металла = (сумма произведений масс каждого изотопа металла на его относительную частоту)
Для расчета атомного веса металла необходимо знать массы всех его изотопов и их относительные частоты в природе.
Для удобства расчета атомного веса металла, существует периодическая система элементов, в которой указаны массы изотопов и отмечены их относительные частоты.
Зная атомный вес металла, можно рассчитать количество атомов металла, содержащихся в определенном количестве вещества. Для этого необходимо использовать формулу:
Количество атомов металла = (масса вещества / атомный вес металла) * число Авогадро
Где число Авогадро равно 6,022 * 10^23 атомов вещества в одном молье.
Таким образом, формула атомного веса металла позволяет рассчитать массу и количество атомов металла, что является важным при изучении свойств и применении металлов в различных областях науки и техники.
Значение атомного веса металла в химических реакциях

Атомный вес металла является важным показателем при проведении химических реакций, так как он определяет количество вещества, которое можно получить из определенного количества металла. Атомный вес металла указывает на массу одного моля металла и измеряется в атомных единицах.
Зная атомный вес металла, можно легко рассчитать количество вещества, которое можно получить после проведения химической реакции. Для расчета количества вещества необходимо знать массу металла и разделить ее на атомный вес. Полученное число будет выражать количество молей вещества.
Атомный вес металла также влияет на процесс образования соединений с другими веществами. Более тяжелые металлы обычно имеют больший атомный вес, что означает, что они обладают большей массой и большей способностью к образованию соединений. Это связано с тем, что атомы таких металлов имеют большее количество электронов и, следовательно, большую химическую активность.
Важно отметить, что атомный вес металла может варьироваться в зависимости от изотопного состава металла. Изотопы могут иметь разную массу и, следовательно, влиять на атомный вес металла. При проведении химических реакций необходимо учитывать изотопный состав металла для более точного расчета количества вещества и предсказания химических свойств соединений.
В заключение, атомный вес металла играет важную роль в химических реакциях, определяя количество вещества и влияя на образование соединений. Точное знание атомного веса металла позволяет проводить расчеты и предсказывать результаты химических процессов, что имеет большое значение в научных и промышленных областях.
Вопрос-ответ

Зачем нужен атомный вес металла?
Атомный вес металла используется для рассчета различных физических и химических свойств, таких как плотность, температура плавления, электропроводность и других.
Как определяется атомный вес металла?
Атомный вес металла определяется путем усреднения массовых чисел атомов различных изотопов этого металла, учитывая их относительные процентные соотношения в природе.
