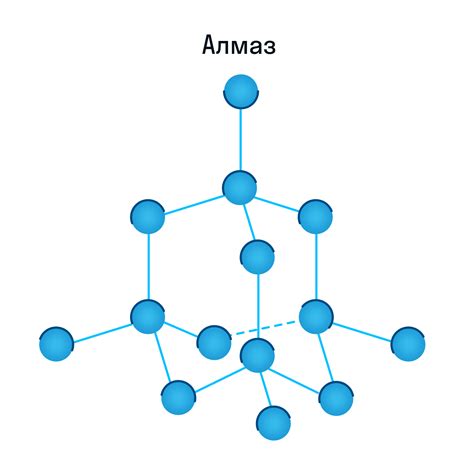
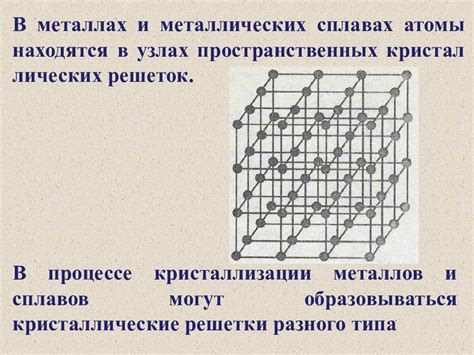
Атомная кристаллическая структура металла – это основа и одно из наиболее важных свойств металлических материалов. Кристаллическая структура обеспечивает металлам их уникальные механические, физические и химические характеристики. В основе атомной структуры лежит регулярное упорядочение атомов в кристаллической решетке. Это упорядочение обеспечивает металлам их прочность, эластичность и способность обладать проводящими свойствами электричества и тепла.
Кристаллическая структура металла формируется благодаря особым свойствам атомов металла и межатомным связям между ними. В кристаллической решетке атомы располагаются в определенном порядке и образуют кристаллическую структуру, которая может быть кубической, гексагональной или другой. В такой упорядоченной структуре атомы металла занимают определенные позиции, называемые узлами решетки.
Особенностью атомной структуры металла является ее высокая устойчивость и возможность изменения при воздействии внешних факторов. Металлы могут подвергаться тепловому воздействию, давлению и прочим условиям, и при этом сохранять свою кристаллическую структуру. Однако, в некоторых случаях, при определенных условиях, металлы могут изменять свою кристаллическую структуру и претерпевать фазовые превращения, что сопровождается изменениями их свойств.
Атомная кристаллическая структура металла
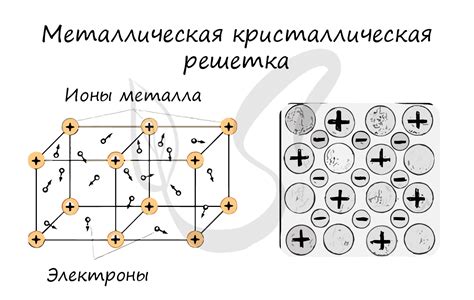
Металлы – это группа материалов, обладающих хорошей проводимостью электрического тока и тепла. Большинство металлов обладает кристаллической структурой, что означает, что их атомы располагаются в определенном порядке.
Атомы в кристаллической структуре металла образуют регулярную решетку. Каждый атом окружен шестью соседними атомами, образуя так называемую кубическую или гексагональную решетку. Эта структура делает металлы прочными и устойчивыми к деформациям.
Уникальные свойства металлов, такие как пластичность, тугоплавкость и хорошая проводимость, связаны с их атомной кристаллической структурой. Благодаря свободным электронам в металлической решетке, металлы обладают высокой электропроводностью и теплопроводностью. Также кристаллическая структура позволяет металлам быть деформируемыми и формировать различные конструкции при обработке.
Атомная кристаллическая структура металла влияет на его механические и физические свойства. Например, образование дислокаций в кристаллической решетке может привести к увеличению прочности металла. Также структура можно модифицировать путем легирования, добавления различных элементов, что позволяет получить специальные свойства металла.
В итоге, атомная кристаллическая структура металла является основой его свойств и предопределяет его поведение в различных условиях. Понимание структуры металла позволяет разрабатывать новые материалы с улучшенными характеристиками и применять их в различных областях техники и промышленности.
Особенности структуры

Атомная кристаллическая структура металла характеризуется наличием упорядоченного расположения атомов в кристаллической решетке. Каждый атом занимает определенное место и имеет соседей, между которыми существуют определенные взаимодействия.
Металлы обладают регулярной сеткой, что означает, что кристаллическая решетка у них однородная и повторяющаяся в пространстве. Такая структура позволяет металлам обладать определенными свойствами, такими как прочность, пластичность и хорошая электропроводность.
Одной из особенностей атомной кристаллической структуры металла является наличие свободных электронов. В металлах электроны находятся на энергетически нижнем уровне, что позволяет им свободно перемещаться в решетке и обеспечивает хорошую электропроводность.
Этот факт также объясняет другое свойство металлов - металлический блеск. При падении света на поверхность металла свободные электроны поглощают энергию от световых волн и переходят на более высокие энергетические уровни. При выходе из металла они испускают фотоны, создавая блеск.
Также структура металлов может включать дефекты, такие как дислокации и грани, которые могут влиять на их физические свойства. Дислокации представляют собой деформации в решетке, а грани - поверхности раздела между кристаллами металла.
Решетка и кристаллические оси
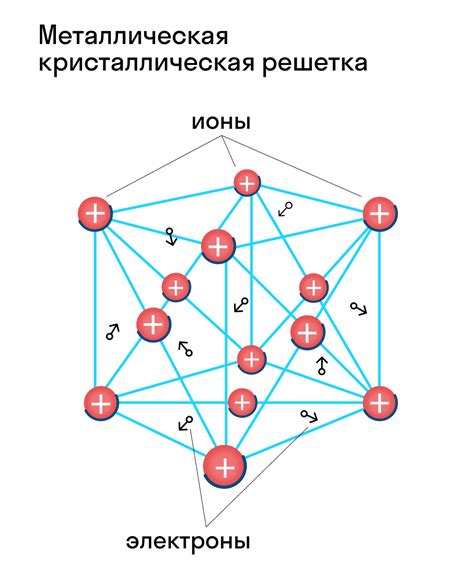
В основе атомной кристаллической структуры металла лежит решетка, представляющая собой трехмерную сетку атомов. Решетка обладает определенной симметрией, которая обеспечивает упорядоченное расположение атомов в кристалле.
В кристаллической решетке можно выделить три оси: ось a, ось b и ось c. Они перпендикулярны друг другу и характеризуют направления в кристаллической структуре. Направление каждой оси определяется отношением расстояний между атомами на этой оси.
Кристаллические оси могут разделяться на основные и дополнительные. Основные оси характеризуют основные направления в решетке и обозначаются буквами a, b, c. Дополнительные оси обозначаются либо цифрами, либо греческими буквами.
Знание кристаллических осей позволяет определять ориентацию кристаллических плоскостей и направления на поверхности металла, что является важным при изучении механических, электрических и других свойств металлов.
Элементарная ячейка
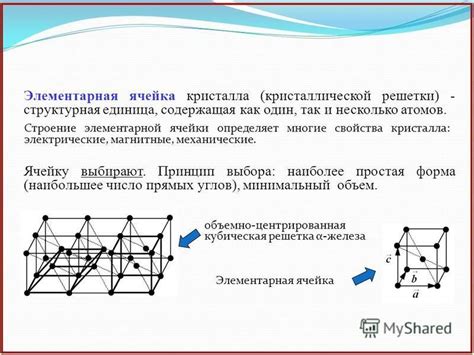
Элементарная ячейка - это фундаментальная структурная единица кристаллической решетки металла. Она обладает всеми симметричными свойствами кристалла и может повторяться бесконечное число раз для формирования всей кристаллической структуры. Элементарная ячейка определяется набором атомов, расположенных в узлах решетки.
В атомных кристаллах металлов элементарная ячейка имеет простую геометрическую форму, которая зависит от типа кристаллической решетки. Обычно применяются три типа решеток: кубическая, гексагональная и тетрагональная. Для каждого типа решетки существует своя элементарная ячейка.
В кубической решетке элементарная ячейка представляет собой куб, в котором каждый угол является узлом решетки, а каждая грань - плоскостью решетки. В гексагональной решетке элементарная ячейка имеет форму призмы или параллелепипеда, у которого основание представляет собой шестиугольник. В тетрагональной решетке элементарная ячейка имеет форму маленького призматического параллелепипеда с четырехугольным основанием.
Элементарная ячейка определяет множество свойств металла, таких как механическая прочность, проводимость электричества и тепла, пластичность и др. Знание структуры элементарной ячейки является важным для понимания межатомных связей в металлах и разработки новых материалов с определенными свойствами.
Металлические связи

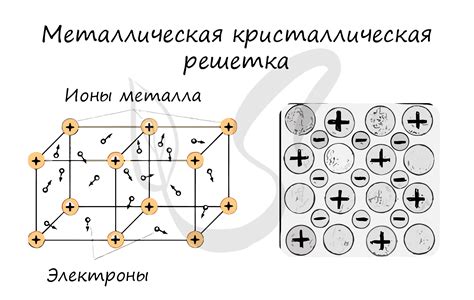
Металлические связи являются особенным типом химической связи, характерным для металлов. В атомной кристаллической структуре металла атомы расположены близко друг к другу и образуют регулярную решетку. Металлы обладают высокой электропроводностью и теплопроводностью благодаря особенностям металлических связей.
Основу металлической связи составляет общий пул свободных электронов, которые передвигаются между атомами металла. Эти свободные электроны образуют так называемое "море электронов". Благодаря этому, металлы обладают высокой электропроводностью, так как электроны могут свободно перемещаться по структуре.
Металлическая связь также обуславливает другие характерные свойства металлов. Например, металлы обладают высокой пластичностью и прочностью. При деформации металла атомы смещаются вокруг своих расположенных близко соседей без разрыва связи. Это позволяет металлам образовывать различные формы и конструкции.
Важно отметить, что металлические связи являются слабыми по сравнению с ионными или ковалентными связями. Это связано с тем, что между атомами металла существует слабые силы взаимодействия. Однако, благодаря большому количеству электронов в "море электронов", металлы обладают высокой внутренней кохезией и прочностью.
Строение и свойства металлов
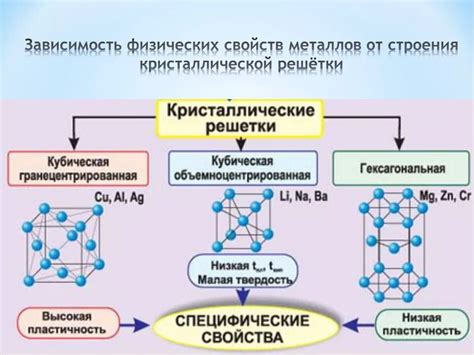
Металлы — это материалы, которые характеризуются особым атомным строением и обладают рядом уникальных свойств. Основой атомной структуры металлов является кристаллическая решетка, состоящая из атомов. Такая решетка обеспечивает металлам прочность и устойчивость к различным нагрузкам.
Атомы в металлах располагаются в виде идеально упорядоченной структуры, где каждый атом имеет своих определенных соседей. Это позволяет металлам обладать высокой пластичностью и способностью к деформации без разрушения. При деформации атомы переносятся на новые позиции, сохраняя при этом связи между соседними атомами и поддерживая целостность материала.
Одной из главных особенностей металлов является их высокая теплопроводность. Это связано с особенностями атомной решетки, которая обеспечивает эффективное распространение тепла по всему объему материала. Также металлы обладают хорошей электропроводностью. Это связано с наличием свободных электронов в атомной решетке, которые могут свободно двигаться и переносить электрический заряд.
Строение металлов также определяет их механические свойства. Металлы обычно обладают высокой прочностью, жесткостью и устойчивостью к износу. Они также могут быть сплавления, что позволяет создавать материалы с различными свойствами в зависимости от состава сплава.
Из-за своих уникальных свойств металлы широко используются в различных отраслях промышленности. Они служат основой для производства множества изделий и конструкций, включая автомобили, самолеты, здания, электронику и многое другое. Благодаря своему строению и свойствам, металлы являются одними из самых важных и неотъемлемых материалов в современном мире.
Дефекты кристаллической структуры
Кристаллическая структура металлов обладает определенным порядком и регулярностью, однако она может содержать различные дефекты, которые влияют на ее свойства и характеристики. Дефекты кристаллической структуры могут быть различных типов и проявляться в виде примесей, вакансий, дислокаций и образования различных окружных и внутрикристаллических пор.
Примеси являются одним из наиболее распространенных типов дефектов кристаллической структуры металлов. Они представляют собой атомы или ионы, замещающие атомы основного металла. Примеси могут влиять на механические и химические свойства металла, изменяя его структуру и состав.
Вакансии – это дефекты, связанные с отсутствием одного или нескольких атомов в кристаллической решетке. Вакансии влияют на плотность и электропроводность металлов, а также на их механическую прочность и термическую стабильность.
Дислокации являются дефектами, связанными с наличием дополнительных плоскостей разрыва внутри металлического кристалла. Они могут быть прямолинейными или закольцованными, а также принимать различные формы и конфигурации. Дислокации влияют на механические свойства металлов, такие как пластичность, твердость и прочность.
Окружные и внутрикристаллические поры являются пространственными дефектами, связанными с наличием полостей и пустот внутри кристаллической структуры металла. Поры влияют на плотность и прочность металлов, а также на их способность к адсорбции и диффузии.
Таким образом, дефекты кристаллической структуры металлов являются неотъемлемой частью их характеристик и свойств. Понимание и контроль этих дефектов позволяет улучшить прочность, пластичность, термическую стабильность и другие значимые свойства металлических материалов и сплавов.
Влияние структуры на свойства металлов
Атомная кристаллическая структура металлов имеет прямое влияние на их свойства и характеристики. Знание и понимание этой связи является необходимым для разработки новых материалов и оптимизации их использования в различных сферах.
Первым важным аспектом влияния структуры на свойства металлов является их кристаллическая упорядоченность. Упаковка атомов в металлах обеспечивает высокую прочность и твердость материала. Деформация кристаллической структуры может привести к изменению механических свойств металла, таких как пластичность, твердость и устойчивость к ударным нагрузкам.
Вторым важным аспектом является наличие дефектов в кристаллической структуре металла. Включения, дислокации и границы зерен могут оказывать влияние на свойства металла, включая его прочность, устойчивость к коррозии и способность к пластической деформации. Исследование и контроль дефектов позволяют улучшить свойства металлов и повысить их производительность в различных условиях эксплуатации.
Третьим значимым фактором влияния структуры на свойства металлов является размер и форма зерен. Мелкозернистые металлы обладают более высокой прочностью и твердостью, а также лучшей устойчивостью к коррозии по сравнению с крупно- и поликристаллическими материалами. Оптимальное соотношение размера и формы зерен позволяет достичь наилучших свойств металлов с учетом конкретных требований и условий эксплуатации.
Итак, структура металлов оказывает значительное влияние на их свойства и позволяет оптимизировать их характеристики для различных целей и задач. Исследование и понимание этого взаимодействия является важным направлением в материаловедении и способствует развитию новых технологий и материалов.
Вопрос-ответ

Что такое атомная кристаллическая структура металла?
Атомная кристаллическая структура металла - это упорядоченное расположение атомов в кристаллической решетке. Она состоит из элементарных ячеек, которые повторяются в пространстве. Эта структура обуславливает свойства металлов, такие как проводимость электричества и тепла, пластичность и т.д.
Какие особенности имеет атомная кристаллическая структура металла?
Атомная кристаллическая структура металла характеризуется регулярным упорядоченным расположением атомов, формированием кристаллической решетки, наличием свободных электронов, обеспечивающих электрическую и тепловую проводимость, а также большой плотностью атомов и плотностью упаковки.
Каковы свойства металлов, обусловленные атомной кристаллической структурой?
Атомная кристаллическая структура металла обуславливает такие свойства металлов, как хорошая электрическая и тепловая проводимость, пластичность, отсутствие прозрачности для света, блеск, магнитные свойства и др.
Какова роль примесей в атомной кристаллической структуре металла?
Примеси влияют на свойства и структуру металла. Они могут изменять кристаллическую решетку, приводить к образованию дополнительных фаз, повышать твердость или деформируемость металла, изменять проводимость электричества и тепла и т.д.
Как можно изменить атомную кристаллическую структуру металла?
Атомную кристаллическую структуру металла можно изменить путем механической обработки, термической обработки, легирования, изменения условий охлаждения и др. Например, обработка металла может привести к возникновению дополнительных дефектов или фаз в структуре, что влияет на его свойства.