Атом переходного металла является особой формой атома, которая обладает уникальными физическими и химическими свойствами. Переходные металлы - это элементы, находящиеся в середине периодической таблицы, между группой 2 и группой 13, включая 3d, 4d, 5d и 6d блоки.
Особенностью атомов переходных металлов является то, что они имеют неполностью заполненные внешние энергетические уровни, что делает их активными химическими элементами. Кроме того, атомы переходных металлов обладают способностью образовывать разнообразные и стабильные соединения, так как имеют несколько возможных вариантов окислительного состояния.
Атомы переходных металлов могут образовывать координационные соединения с другими атомами или ионами, в которых атом переходного металла играет роль центрального ионного комплекса. Эти соединения обладают различными физическими свойствами и широко используются в различных областях, таких как каталитическое вещество, магнитные материалы, лекарственные препараты и многое другое.
Атом переходного металла: структура и свойства
Переходные металлы представляют собой элементы в десятой и одиннадцатой группах периодической таблицы, а также в группах с 3 по 12. Атом переходного металла имеет сложную структуру и обладает уникальными свойствами.
Структура атома переходного металла отличается от структуры атома простых металлов. Внутренние энергетические уровни атома переходного металла заполняются несколько сложнее, с учетом возможности образования половинно заполненных и дублетных состояний. Это связано с особенностями расположения электронов в d-орбитали, благодаря чему возможны разные конфигурации энергетических уровней.
Одной из особенностей атомов переходных металлов является их способность образовывать комплексы с другими атомами или ионами. Здесь важную роль играют д-орбитали, которые обеспечивают наличие свободных электронов для образования связей с другими атомами. Это позволяет переходным металлам образовывать стабильные соединения разной степени окисления и свойства, такие как цветность и магнитные свойства.
Свойства атома переходного металла также определяют его химическую активность. Она может варьироваться в зависимости от числа электронов в d-орбиталях и реакционной способности атома. Некоторые переходные металлы являются хорошими катализаторами, способными ускорять химические реакции на поверхности своего атома. Другие же переходные металлы обладают высокой степенью стабильности и устойчивости к окислению.
В заключение, атом переходного металла имеет сложную структуру и проявляет уникальные свойства. Расположение электронов в d-орбиталях обеспечивает возможность образования комплексов и варьирующуюся химическую активность. Переходные металлы играют важную роль в множестве химических, физических и биологических процессах.
Структура атома переходного металла и его влияние на свойства
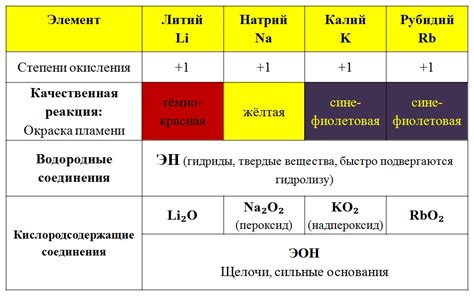
Переходные металлы – это элементы химической группы, расположенной в периодической системе после щелочно-земельных металлов. Они характеризуются особыми свойствами, которые обусловлены структурой активного атома и его электронной конфигурацией.
Одной из особенностей структуры атома переходного металла является наличие у него внутренней электронной оболочки, которая заполняется перед внешней оболочкой. Это приводит к образованию зон проводимости и валентной зоны. Следует отметить, что электроны в зоне проводимости могут двигаться свободно, что обусловливает металлические свойства переходных металлов.
Кроме того, атомы переходных металлов имеют сложную валентность, что означает, что они могут образовывать соединения с различными степенями окисления. Это связано с постепенным заполнением d-электронной оболочки, что приводит к возможности перехода электрона из одного d-орбиталя в другой.
Структура атома переходного металла сказывается на его физических и химических свойствах. Например, наличие свободно движущихся электронов в зоне проводимости позволяет переходным металлам иметь высокую электропроводность и теплопроводность. Кроме того, их сильная способность образовывать соединения позволяет им обладать широкими возможностями для образования различных соединений и координационных соединений.
Таким образом, структура атома переходного металла имеет существенное влияние на его свойства, обусловленные как электронной конфигурацией, так и сложной валентностью этих элементов.
Химические свойства атома переходного металла: реакционная способность и катализ

Атомы переходных металлов обладают разнообразными химическими свойствами, которые определяют их реакционную способность и способность катализировать химические реакции.
Во-первых, атомы переходных металлов обладают переменным окислительным состоянием, что позволяет им участвовать в различных реакциях. Они могут образовывать соединения с различными степенями окисления, что открывает широкие возможности для образования различных химических связей.
Во-вторых, атомы переходных металлов часто обладают высокой каталитической активностью. Они способны ускорять химические реакции, не участвуя в них сами. Катализ переходных металлов может происходить как в газовой фазе, так и в жидкостях и растворах. Это свойство атомов переходных металлов нашло широкое применение в промышленности и лабораторных условиях.
Каталитические свойства атомов переходных металлов особенно важны в реакциях окисления и восстановления, где они могут участвовать как окислители или восстановители. Благодаря своей способности принимать и переходить между различными степенями окисления, атомы переходных металлов могут эффективно участвовать в межмолекулярных превращениях.
Кроме того, атомы переходных металлов могут образовывать сложные координационные соединения, в которых они образуют стабильные комплексы с другими атомами или группами атомов. Эти соединения могут также обладать каталитической активностью и использоваться для проведения различных химических превращений.
В целом, химические свойства атома переходного металла обусловлены его электронной структурой, которая позволяет ему образовывать разнообразные связи и участвовать в различных реакциях. Эти свойства делают атомы переходных металлов ценными компонентами в химической промышленности и исследовательской деятельности.
Физические свойства атома переходного металла: электропроводность и магнитные свойства

Атом переходного металла обладает рядом особенных физических свойств, которые отличают его от атомов других элементов. Одно из основных свойств атома переходного металла - это его высокая электропроводность. Это означает, что атомы переходного металла способны передавать электрический заряд с большой эффективностью. Это возможно благодаря особой структуре энергетических уровней в атоме переходного металла.
Одной из причин высокой электропроводности атома переходного металла является наличие свободных электронов в его внешних энергетических оболочках. Эти свободные электроны могут передвигаться по объему металла, образуя так называемое "море электронов". Именно наличие этого "моря электронов" обуславливает высокую электропроводность переходных металлов.
Кроме того, атом переходного металла обладает также высокими магнитными свойствами. В зависимости от конкретного переходного металла, атом может образовывать различные типы магнитных состояний. Например, некоторые переходные металлы, такие как железо и никель, образуют ферромагнитные материалы, которые проявляют сильное притяжение к магнитному полю.
Однако, не все переходные металлы обладают магнитными свойствами. Некоторые из них, такие как медь и цинк, являются диамагнитными материалами, что означает, что они имеют слабое отталкивающее взаимодействие с магнитным полем.
Таким образом, атом переходного металла характеризуется высокой электропроводностью и различными магнитными свойствами, в зависимости от конкретного металла. Эти особенности делают переходные металлы важными материалами для различных промышленных и научных приложений.
Вопрос-ответ

Что такое атом переходного металла?
Атом переходного металла - это атом элемента, который находится в д-блоке периодической таблицы. Он обладает особенностями, которые отличают его от атомов других элементов.
Какие особенности имеет атом переходного металла?
Атом переходного металла имеет несколько особенностей. Во-первых, у него нарушается правило восеми электронов в валентной оболочке, что позволяет ему образовывать различные степени окисления. Во-вторых, у атома переходного металла имеется неполная d-оболочка, что позволяет ему образовывать комплексные соединения и проявлять каталитическую активность. Еще одной особенностью является возможность образования различных изомеров.
