Внешний электронный уровень атома металла играет важную роль в его химических свойствах и реактивности. Он состоит из электронов, находящихся на самом удаленном от ядра уровне. Электронная формула внешнего уровня атома металла позволяет определить количество электронов на этом уровне и, следовательно, его возможности к образованию химических связей.
Высший оксид металла, также известный как оксид X уровня Me2O3, представляет собой химическое соединение, в котором металл играет роль катиона, а кислород — аниона. Электронная формула внешнего уровня атома металла позволяет определить, сколько электронов на самом удаленном от ядра уровне атома металла участвует в образовании химической связи с атомами кислорода в высшем оксиде.
Определение электронной формулы внешнего уровня атома металла и высшего оксида Me2O3 открывает возможности для изучения его химических свойств и возможностей в реакциях с другими веществами. Это позволяет предсказывать поведение вещества при различных условиях и его возможности в реагировании с другими соединениями, что является важным фактором в химической промышленности и научных исследованиях.
Определение электронной формулы внешнего уровня атома металла и его высший оксид Me2O3

Электронная формула внешнего уровня атома металла и его высший оксид Me2O3 определяется с помощью анализа электронной структуры атома и составления соответствующей химической формулы. Электронная формула позволяет понять, какие электроны металлического атома участвуют в химических реакциях и какие оксиды образуются при взаимодействии металла с кислородом.
Внешний уровень атома металла содержит валентные электроны, которые определяют химическую активность металла. Они находятся на самом удаленном от ядра энергетическом уровне и определяют способность металла образовывать химические связи с другими атомами. Число валентных электронов определяет химическую группу, к которой принадлежит металл в периодической системе элементов.
Высший оксид металла Me2O3 является соединением металла и кислорода, где металл имеет наивысшую степень окисления. В оксиде Me2O3 каждый атом металла соединен с тремя атомами кислорода. Такая формула позволяет определить стехиометрическое соотношение между металлом и кислородом в соединении и его общую зарядовую структуру. Электронная формула внешнего уровня атома металла и его высший оксид Me2O3 позволяет представить химические свойства и реакционную способность данного соединения.
Внешний уровень атома и его значение для химических связей

Внешний уровень атома – это самый дальний от ядра электронный уровень. Он содержит валентные электроны, которые участвуют в образовании химических связей. Структура внешнего уровня атома определяет его химические свойства.
Количество электронов на внешнем уровне для атомов металлов определяется по номеру группы в Периодической системе Менделеева. Например, вторая группа содержит два электрона на внешнем уровне, третья группа – три электрона и т.д.
Внешний уровень атомов металлов играет важную роль в образовании химических связей. Электроны валентной оболочки металла могут активно участвовать в обмене электронами с другими атомами. Они могут быть переданы несколькими способами – образуя ионные, ковалентные или металлические связи.
Высший оксид металла Me2O3 образуется при взаимодействии атомов металла с кислородом. В этом соединении все валентные электроны металла участвуют в связях с кислородом. Количество кислородных атомов, а соответственно, их связей с металлом определяется восхождением в Периодической системе Менделеева.
Внешний уровень атома металла и его высший оксид Me2O3 имеют принципиальное значение для понимания химических свойств этих веществ и их применения в различных областях науки и техники.
Электронная формула и способы ее определения для атомов металла

Электронная формула является записью количества электронов, находящихся на каждом энергетическом уровне атома металла. Она позволяет наглядно представить распределение электронов по оболочкам и подобрать соответствующий способ, чтобы определить ее.
Существует несколько методов для определения электронной формулы атома металла. Один из них основан на заполнении энергетических уровней электронами по низлежащим принципам. Сначала заполняются внутренние энергетические оболочки, а затем внешняя оболочка, отвечающая за валентность. Такой метод позволяет получить формулу с помощью систематического подхода.
Второй способ основывается на использовании системы периодического расположения элементов. Зная атомный номер металла или его положение в таблице элементов, можно определить количество электронов на каждом энергетическом уровне. Этот метод быстр и эффективен, не требует проведения сложных вычислений.
Также существуют специальные таблицы, которые содержат информацию о количестве электронов на каждом энергетическом уровне для различных элементов. С их помощью можно быстро определить электронную формулу атома металла без необходимости проведения сложных вычислений или изучения периодической системы элементов.
Электронная формула является важным инструментом для изучения свойств и характеристик металлов, а также их соединений. Она позволяет определить валентность атома, его способность к образованию ионов и место в периодической системе элементов.
Металлы и их оксиды Me2O3: свойства и применение

Металлы - вещества, обладающие хорошей проводимостью электричества и тепла, обычно с блестящей поверхностью.
Оксиды металлов Me2O3 - химические соединения, состоящие из металлического и кислородного атомов. Они имеют большую важность в различных областях науки и техники.
Основные свойства металлов и их оксидов Me2O3:
- Проводимость электричества и тепла. Металлы и оксиды Me2O3 обладают высокой электрической и тепловой проводимостью, что делает их ценными материалами в электронике и промышленности.
- Пластичность и гибкость. Металлы могут быть легко формованы и изгибаемы, что позволяет использовать их в различных конструкциях и изделиях.
- Высокая плотность. Металлические оксиды Me2O3 обладают высокой плотностью, что позволяет использовать их в изготовлении тяжелых конструкций и инструментов.
- Неонный блеск. Металлы и их оксиды Me2O3 обладают блестящей поверхностью, что делает их эстетически привлекательными материалами для украшений и декоративных изделий.
Применение металлов и их оксидов Me2O3:
- Производство металлургических материалов. Металлы и их оксиды Me2O3 используются для создания сплавов и сталей с различными механическими и химическими свойствами.
- Электронная промышленность. Металлы и их оксиды Me2O3 используются для создания различных электронных компонентов, таких как проводники, контакты и электроды.
- Строительство. Металлы и их оксиды Me2O3 используются для создания прочных и долговечных конструкций, например, в производстве металлических рамок и строительных фундаментов.
- Декоративное искусство и украшения. Металлы и их оксиды Me2O3 широко используются для создания ювелирных изделий, скульптур и других декоративных элементов.
Металлы и их оксиды Me2O3 играют важную роль в различных отраслях науки и техники, обладая свойствами, которые делают их ценными материалами для множества применений.
Физические и химические свойства оксидов Me2O3

Оксиды Me2O3 – это химические соединения, образованные металлами группы земель Me и кислородом. Они являются высшими оксидами соответствующих металлов и имеют общую структурную формулу Me2O3, где Me обозначает металл группы земель.
Физические свойства оксидов Me2O3 зависят от конкретного металла, который входит в их состав. Например, оксиды алюминия (Al2O3) и кремния (SiO2) являются кристаллическими веществами с высокой температурой плавления. Однако, оксиды таких металлов, как индий (In2O3) и железо (Fe2O3), обладают более низкими температурами плавления и имеют аморфную структуру.
Химические свойства оксидов Me2O3 включают реакцию с водой, кислотами и щелочами. Взаимодействие оксидов Me2O3 с водой неравновесно, они образуют основания. Например, окисление воды с образованием гидроксида натрия (NaOH) происходит при реакции между оксидом натрия (Na2O) и водой.
Реакция оксидов Me2O3 с кислотами дает соли. Например, реакция между оксидом кальция (CaO) и серной кислотой (H2SO4) приводит к образованию сульфата кальция (CaSO4).
Кроме того, оксиды Me2O3 могут проявлять свойства оптических материалов. Например, при добавлении примесей определенных элементов, таких как иттрий (Y), европий (Eu) или дейтерий (Dy), оксид индия (In2O3) может обладать фосфоресцентными свойствами и использоваться в различных электронных устройствах и дисплеях.
Способы получения оксидов Me2O3
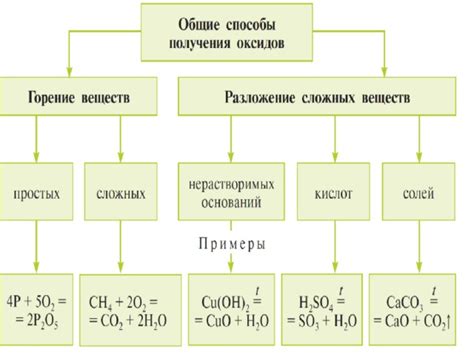
Оксиды типа Me2O3 могут быть получены различными способами, в зависимости от свойств и химической активности металла Me. Рассмотрим некоторые из них.
- Термическое окисление металла: одним из наиболее распространенных способов получения оксидов Me2O3 является термическое окисление металлического металла Me при высоких температурах. Например, в случае железа (Fe), для получения оксида Fe2O3 необходимо нагревать металл до температуры около 800°C в присутствии кислорода.
- Химическое воздействие: некоторые металлы Me могут образовывать оксиды Me2O3 путем химического воздействия на другие вещества. Например, оксид хрома (Cr2O3) получают путем воздействия хроматной кислоты (H2CrO4) на хромовую краску (Cr2O3).
- Электролиз: для получения оксидов Me2O3 также может использоваться метод электролиза. Это особенно характерно для металлов, которые могут быть электролитически окислены. Например, для получения оксида алюминия (Al2O3) применяется электролиз расплава алюминия в присутствии подходящего электролита.
Способы получения оксидов Me2O3 могут быть различными и определяются как свойствами металла Me, так и требуемыми условиями реакции. Знание этих способов является важным для химиков и исследователей, работающих в области синтеза новых материалов и разработке новых технологий.
Применение оксидов Me2O3 в промышленности и научных исследованиях

Оксиды Me2O3, где Me обозначает металл, имеют широкое применение и в промышленности, и в научных исследованиях. Эти оксиды обладают рядом полезных свойств, которые делают их востребованными в различных областях.
Одним из главных применений оксидов Me2O3 является использование их в качестве катализаторов в химической промышленности. Эти оксиды могут повысить скорость химических реакций, обеспечивая более эффективное протекание процессов. Благодаря этому, оксиды Me2O3 находят применение в производстве различных химических веществ, фармацевтике, и производстве пластиков и полимеров.
Оксиды Me2O3 также активно применяются в электронике и солнечной энергетике. Их электропроводимость делает их идеальными материалами для создания полупроводниковых компонентов и солнечных элементов. Благодаря своим электрическим свойствам, оксиды Me2O3 также применяются в производстве электронных устройств и микросхем.
В научных исследованиях оксиды Me2O3 играют важную роль. Они используются для исследования различных свойств материалов и в процессе создания новых материалов с улучшенными свойствами. Оксиды Me2O3 также применяются в качестве покрытий для защиты поверхностей материалов от окисления и коррозии.
Объем применения оксидов Me2O3 в различных областях становится все более значительным, благодаря их полезным свойствам и возможностям. Эти оксиды находят все большее применение в промышленности и научных исследованиях, что делает их важными компонентами в различных технологиях и процессах.
Вопрос-ответ

Какую электронную формулу имеет внешний уровень атома металла в оксиде Me2O3?
Внешний уровень атома металла в оксиде Me2O3 имеет электронную формулу 3s23p6.
Какая электронная формула высшего оксида Me2O3?
Высший оксид Me2O3 имеет электронную формулу O2-.
