Амфотерные металлы представляют собой класс элементов, которые обладают способностью образовывать соединения с различными химическими соединениями. Они могут проявлять как основные, так и кислотные свойства, взаимодействуя как с кислотами, так и с основаниями.
К таким металлам относятся, например, алюминий, цинк, железо и медь. Они могут образовывать комплексные соединения, в которых практически все атомы металлов образуют связи с молекулами других веществ. Это делает их особенно важными во многих областях, включая промышленность, медицину и сельское хозяйство.
Одним из примеров амфотерных металлов является алюминий. Он может проявлять и кислотные, и основные свойства. С одной стороны, он может взаимодействовать с кислотами, образуя с ними соли. С другой стороны, он может реагировать с основаниями, образуя гидроксиды. Алюминиевые соединения широко используются в производстве лёгких сплавов, строительных материалов и в косметике.
Амфотерные металлы являются важными элементами химического мира. Их способность образовывать разнообразные соединения делает их незаменимыми для многих отраслей науки и промышленности. Их свойства позволяют создавать материалы с уникальными характеристиками и использовать их в сфере новых технологий.
Другим примером амфотерного металла является цинк. Он также может проявлять и кислотные, и основные свойства. Цинк является необходимым микроэлементом для организма человека и играет важную роль в ряде биологических процессов. Он также широко используется в металлообработке, электротехнике и в производстве аккумуляторов и керамики.
Все амфотерные металлы имеют уникальные свойства и широкий спектр применения. Их способность образовывать разнообразные соединения позволяет использовать их в различных областях науки и технологий. Их важность в современном мире трудно переоценить, ведь они являются ключевыми компонентами многих процессов и продуктов, которые окружают нас повседневно.
Амфотерные металлы в химии
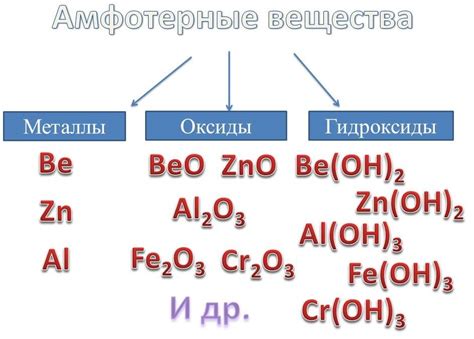
Амфотерные металлы - это класс элементов, которые способны образовывать разнообразные соединения как с кислородными, так и с основными свойствами. Эти элементы проявляют себя как кислоты, реагируя с основаниями, и как основания, реагируя с кислотами. Таким образом, амфотерные металлы имеют свойство разнонаправленной реакции в зависимости от окружающей среды и типа вещества, с которым они взаимодействуют.
Типичным примером амфотерного металла является алюминий (Al). Он может действовать как кислота, реагируя с основаниями и образуя соли, например, алюминаты. В то же время, алюминий может также проявлять основные свойства, реагируя с кислотами и образуя алюминатные ионы.
Другим примером амфотерного металла является цинк (Zn). Он может реагировать как с кислотами, так и с основаниями, образуя соответствующие соли. Например, цинк может реагировать с соляной кислотой, образуя хлорид цинка, а также с гидроксидом натрия, образуя гидроксид цинка.
Амфотерные металлы играют важную роль в ряде химических и промышленных процессов. Они могут быть использованы в производстве различных продуктов, таких как лекарства и косметические препараты, а также в процессах катализа и обработки материалов.
Основные характеристики и свойства амфотерных металлов
1. Определение:
Амфотерные металлы - это элементы, обладающие способностью образовывать соединения с различными кислотами и основаниями. Они могут проявлять свойства исключительно кислоты или исключительно основания, в зависимости от условий реакции.
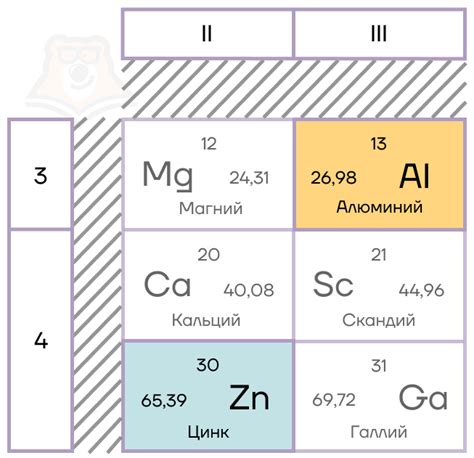
2. Примеры амфотерных металлов:
К наиболее известным амфотерным металлам относятся алюминий (Al), цинк (Zn), свинец (Pb), железо (Fe), гидроксиды которых обладают и кислотными, и основными свойствами.
3. Реакция с кислотами:
Амфотерные металлы противодействуют кислотам, образуя с ними соли. В этом случае они проявляют свои особенности в роли основания и принимают на себя протоны от кислоты.
4. Реакция с основаниями:
В реакции с основаниями амфотерные металлы проявляют свойства кислоты, отдавая свои протоны базе и образуя соль.
5. Способность к образованию амфотерных оксидов:
Одной из важных характеристик амфотерных металлов является способность образовывать амфотерные оксиды, которые могут реагировать как с кислотами, так и с основаниями.
6. Применение:
- Амфотерные металлы часто используются в процессах обработки воды, поскольку их соединения способны нейтрализовать кислоты и основания, повышающие или понижающие pH водных растворов.
- Они также имеют применение в производстве косметических и фармацевтических препаратов, поскольку способны воздействовать на кислотно-щелочной баланс организма.
- Амфотерные металлы находят применение в производстве электроники и катализаторов, благодаря своим особым свойствам.
Химические соединения и реакции

Амфотерные металлы являются важными компонентами многих химических соединений и участвуют в различных химических реакциях. Они обладают способностью образовывать разнообразные соединения как с кислотами, так и с основаниями.
Амфотерные металлы могут образовывать соли с кислотами, при этом они выступают в роли оснований. Например, амфотерный металл алюминий может образовывать соль алюминия с кислотами, такими как соляная кислота или серная кислота.
Одновременно амфотерные металлы проявляют основательные свойства и образуют гидроксиды с кислотными оксидами. Например, оксид амфотерного металла железа реагирует с водой, образуя гидроксид железа (III).
В химических реакциях амфотерные металлы могут выступать в роли окислителей или восстановителей в зависимости от условий. Например, хромат амфотерного металла хрома может взаимодействовать с серной кислотой в кислой среде, окисляясь до хромовой кислоты, либо взаимодействовать с кислородом в основной среде, восстанавливаясь до иона хрома (III).
Вопрос-ответ

Какие металлы являются амфотерными и способны образовывать разнообразные соединения?
Амфотерными металлами являются, например, алюминий, железо и цинк. Они способны образовывать соединения как с кислотами, так и с основаниями.
Как амфотерные металлы образуют соединения с кислотами?
Амфотерные металлы образуют соединения с кислотами путем присоединения к ним оксидных групп или анионов. В результате образуется соль металла и кислоты.
Как амфотерные металлы образуют соединения с основаниями?
Амфотерные металлы образуют соединения с основаниями путем присоединения к ним гидроксильных групп или катионов. В результате образуется соль металла и основания.
Каким образом амфотерные металлы проявляют свою амфотерность?
Амфотерные металлы проявляют свою амфотерность путем возможности образования как кислотных, так и основных соединений. Это связано с их способностью присоединяться как к кислотам, так и к основаниям.
