Аллотропия металлов – это явление изменения структуры и физических свойств металла при различных условиях. В результате аллотропических превращений металл может образовывать различные модификации, называемые аллотропами. Каждый аллотроп обладает уникальными свойствами и может иметь значительное влияние на его применение в различных областях науки и промышленности.
Примером аллотропии металлов может служить железо. При комнатной температуре железо обладает аустенитной структурой, которая обеспечивает ему прочность и твердость. Однако, при нагревании до высоких температур, железо претерпевает аллотропное превращение и образует ферритную структуру, которая обладает более мягкими свойствами. Этот факт широко используется в металлургической промышленности при обработке стали.
Еще одним примером аллотропии является серебро. Оно может существовать в двух различных аллотропных модификациях – альфа-серебре и бета-серебре. Альфа-серебро обладает кубической решеткой, а бета-серебро – ромбической. Каждая из этих модификаций имеет свои уникальные свойства и структуру, что делает серебро интересным и практически незаменимым материалом в различных отраслях, включая ювелирное и электронное производство.
Аллотропия металлов является важным понятием в науке и инженерии, так как позволяет понять и контролировать изменение свойств металлов при изменении условий их эксплуатации. Изучение аллотропии металлов позволяет создавать новые материалы с уникальными свойствами и использовать их в различных областях человеческой деятельности.
Что такое аллотропия металлов и каковы ее особенности?

Аллотропия металлов – это явление, при котором один и тот же химический элемент может существовать в различных физических формах, называемых аллотропными модификациями металла. Аллотропия — это свойство некоторых элементов в твердом состоянии при разных температурах и давлениях образовывать различные модификации с разными структурами и свойствами.
Аллотропные модификации металлов могут различаться по структуре, электронной конфигурации, силе валентных связей, твердости, электропроводности и другим свойствам. Часто аллотропные модификации обладают разными физическими и химическими свойствами, что позволяет использовать их в различных областях науки и промышленности.
Примерами металлической аллотропии являются железо и углерод. Железо может существовать в альфа- и гамма-модификациях, которые различаются по структуре и свойствам. Углерод может образовывать аллотропные модификации в виде алмаза и графита, каждая из которых имеет свою уникальную структуру и свойства.
Особенностью аллотропии металлов является то, что различные модификации металла обладают разными свойствами, что позволяет использовать их в различных областях. Например, гамма-модификация железа обладает более высокой твердостью и прочностью, чем альфа-модификация, что делает ее идеальным материалом для изготовления инструментов и механизмов.
Определение аллотропии металлов
Аллотропия металлов - это явление, при котором один и тот же химический элемент может существовать в разных структурных состояниях, называемых аллотропными модификациями. Каждая аллотропная модификация металла обладает своими уникальными свойствами и физическими характеристиками.
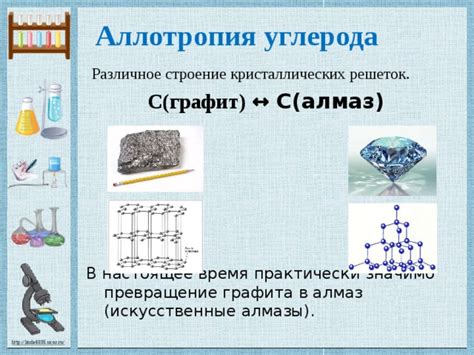
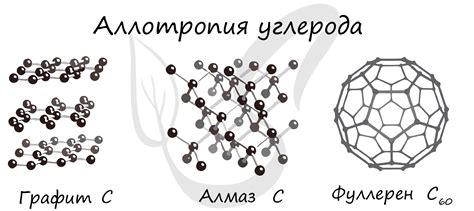
Примерами аллотропных модификаций металлов являются различные формы углерода, такие как графит, алмаз и фуллерены. Аллотропные модификации металлов могут отличаться по кристаллической структуре, плотности, цвету, химической активности и другим свойствам.
Аллотропия металлов является результатом особенностей взаимодействия атомов металла в кристаллической решетке. Изменение условий температуры и давления может приводить к изменению аллотропной модификации металла. Некоторые металлы могут обладать более чем одной аллотропной модификацией, в то время как другие металлы имеют только одну аллотропную модификацию.
Примеры аллотропии металлов в природе

Железо. Одной из наиболее известных и широко распространенных форм аллотропии в металлах является железо. Оно может существовать в разных структурах, включая кубическую структуру центрированного гранецентрированного (бипироаморфного) железа и кубическую структуру гранецентрированного железа. Каждая форма имеет свои уникальные свойства, такие как твердость и магнитные характеристики.
Медь. Еще одним примером аллотропии металлов является медь. Она может существовать в двух основных структурах: кубической гранецентрированной и кубической пространственно центрированной. Кубическая гранецентрированная медь имеет высокую электропроводимость и используется в проводах и электрических устройствах, в то время как кубическая пространственно центрированная медь используется, например, в ювелирных изделиях.
Свинец. Свинец также проявляет аллотропию и может существовать в трех структурах: кубической, ромбической и тетрагональной. Каждая из этих структур имеет разные физические свойства. Например, ромбический свинец является мягким и пластичным, в то время как кубический свинец более твердый и хрупкий.
Углерод. Необходимо также упомянуть аллотропию металлического элемента - углерода. Углерод может существовать в нескольких формах, включая алмаз, графит и фуллерен. Каждая из этих структур имеет свои уникальные свойства, такие как твердость, электропроводность и теплопроводность. Например, алмаз является одним из самых твердых известных материалов, графит - отличный проводник электричества, а фуллерены обладают уникальными молекулярными свойствами.
Примеры искусственной аллотропии металлов
Искусственная аллотропия металлов - это процесс изменения структуры и свойств металлов путем создания специальных условий с использованием различных методов.
Одним из примеров искусственной аллотропии металлов является получение аморфного металла. Аморфные металлы отличаются от кристаллических своей структурой. В процессе получения аморфного металла металлический материал быстро охлаждается, что не дает кристаллам образовываться. Таким образом, аморфный металл имеет более высокую прочность и другие уникальные свойства.
Еще одним примером искусственной аллотропии металлов являются сплавы. Сплавы - это материалы, состоящие из двух или более металлов или металла и других веществ. В процессе создания сплавов металлы могут испытывать изменения в своей структуре и свойствах, что позволяет получить материалы с различными характеристиками. Например, сплавы могут иметь повышенную прочность, жаропрочность или коррозионную стойкость.
Еще одним интересным примером искусственной аллотропии металлов является создание наноматериалов. Наноматериалы - это материалы с размерами частиц в пределах нанометров. Путем изменения размеров частиц металлов можно добиться изменения их свойств. Наноматериалы имеют большую площадь поверхности, что делает их уникальными для использования в различных областях, например, в катализе или электронике.
Таким образом, искусственная аллотропия металлов представляет собой широкий спектр методов исследования и производства материалов с измененными свойствами. Она позволяет получать материалы с новыми уникальными характеристиками, которые могут быть применены в различных областях науки и промышленности.
Особенности аллотропной модификации металлов
Аллотропия металлов – это свойство некоторых металлов образовывать различные структурные формы в зависимости от условий окружающей среды. Одним из примеров аллотропных модификаций является железо, которое может быть в форме альфа-железа, гамма-железа и дельта-железа.
Каждая из аллотропных модификаций железа имеет свои характеристики. Например, альфа-железо имеет кубическую решетку, высокую плотность и обладает магнитными свойствами. Гамма-железо, в свою очередь, обладает более сложной кристаллической структурой и способно выдерживать высокие температуры без изменения своих свойств.
Одной из причин аллотропии металлов является изменение их электронной структуры под воздействием различных факторов, таких как давление, температура или добавление легирующих элементов. В результате изменения электронной структуры меняются и физические свойства металла, такие как термическая и электрическая проводимость, твердость и пластичность.
Аллотропия металлов имеет широкое практическое применение. Например, аллотропная модификация железа используется в производстве стали, где путем изменения содержания и условий кристаллизации можно получить материал с определенными механическими и магнитными свойствами. Понимание особенностей аллотропных модификаций металлов позволяет улучшать их технологические и эксплуатационные характеристики и применять их в различных отраслях промышленности.
Роль аллотропии металлов в промышленности

Аллотропия, или способность металлов образовывать различные аллотропные модификации, играет важную роль в различных отраслях промышленности.
В первую очередь, аллотропные модификации металлов являются строительным материалом для создания различных конструкций и изделий в строительной промышленности. Например, железо может быть использовано как сталь, чугун или сплавы с другими металлами, такими как никель или медь, для создания прочных и устойчивых к разрушению строительных конструкций.
Благодаря аллотропии, металлы также находят широкое применение в автомобильной промышленности. Аллюминий, к примеру, может быть использован в виде прочного и легкого материала для создания кузовов автомобилей, что позволяет уменьшить вес автомобиля и увеличить его энергоэффективность.
Аллотропия металлов играет также важную роль в химической промышленности. Например, каталитическое применение платины в различных химических процессах возможно благодаря ее способности образовывать аллотропные модификации с повышенной активностью катализатора.
И, наконец, аллотропные модификации металлов используются в электронной промышленности. Германий, например, может быть использован в виде полупроводника для создания различных электронных компонентов, таких как транзисторы и диоды.
Вопрос-ответ

Какие примеры металлов существуют в разных аллотропных формах?
Некоторые примеры металлов, которые могут существовать в разных аллотропных формах, включают железо, углерод и кислород. Другими примерами являются медь, никель и цинк.
Чем характеризуется аллотропия металлов?
Аллотропия металлов характеризуется способностью металла существовать в разных аллотропных формах, в которых его атомы или ионы имеют различную структуру или упорядочение. Это может привести к разным физическим и химическим свойствам металла в каждой аллотропной форме.
