Металлы - это удивительный класс материалов, который известен человечеству уже на протяжении тысячелетий. Они обладают множеством уникальных свойств, таких как высокая теплопроводность и электропроводность, прочность и пластичность. Однако, что делает металлы еще более удивительными, это их способность к аллотропии - возможность принимать различные кристаллические структуры при одном и том же химическом составе.
Аллотропия металлов представляет собой явление, при котором один и тот же элемент может образовывать несколько различных модификаций с разными физическими и химическими свойствами. Это связано с особенностями внутренней структуры кристаллической решетки металлов. Изменение условий окружающей среды, таких как температура и давление, может привести к изменению кристаллической структуры металла и, соответственно, к изменению его свойств.
Примером аллотропии металлов является железо. При комнатной температуре оно обычно находится в альфа-железной модификации, которая обладает относительно низкой твердостью. Однако, при нагревании до определенной температуры, альфа-железо превращается в бэта-железо с более высокой твердостью и прочностью. Также, железо может образовывать гамма-железо при высоких температурах, которое обладает еще более удивительными свойствами, такими как суперпластичность и способность к деформации без разрушения.
Аллотропия металлов: разнообразие структур и свойств
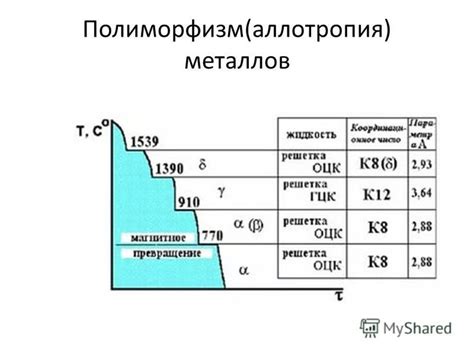
Аллотропия – это свойство некоторых химических элементов образовывать вещества с различными кристаллическими структурами. Металлы не являются исключением: они тоже могут образовывать различные аллотропные модификации.
Основные примеры аллотропии металлов – железо, углерод и сера. Железо, например, может существовать в трех основных модификациях: альфа-железо, гамма-железо и дельта-железо. Альфа-железо является стабильной при комнатной температуре и обладает кубической решеткой. Гамма-железо образуется при нагреве выше 912 °C и также имеет кубическую решетку. Дельта-железо образуется при нагреве свыше 1392 °C и обладает тетрагональной решеткой.
Углерод, в зависимости от условий синтеза, может образовывать аллотропные модификации - графит и алмаз. Графит представляет собой слоистую структуру, состоящую из шестиугольных слоев, обладает мягкостью и проводит электричество. Алмаз же образуется под действием высокого давления и температуры, имеет кристаллическую решетку и является одним из самых твердых и прочных материалов.
Еще одним примером аллотропии металлов является сера, которая может быть представлена двумя главными формами: ромбической и моноклинной. Ромбическая сера образуется при температуре ниже 95,3 °C и имеет легкую твердую фазу. Моноклинная сера образуется при температурах выше 95,3 °C и является пластичной и мягкой.
Что такое аллотропия металлов?

Аллотропия металлов — это свойство некоторых металлических элементов образовывать различные структуры и фазы в разных условиях. Аллотропия является результатом изменения атомного или молекулярного строения металла без изменения его химического состава.
Аллотропные формы металлов могут отличаться по кристаллической структуре, плотности, термической и электрической проводимости, магнитных свойствах и т. д. Некоторые металлы образуют множество аллотропных форм, которые могут сохраняться при различных давлениях и температурах.
Например, ужелезо может существовать в трех аллотропных формах: альфа-железо, гамма-железо и дельта-железо. Альфа-железо является стабильной формой при комнатной температуре и обычном давлении. Гамма-железо обладает более высокой температурной стабильностью и является структурной формой при повышенных температурах. Дельта-железо образуется при очень высоких температурах.
Аллотропия металлов является важным явлением, которое влияет на их использование в различных областях, таких как металлургия, электроника и строительство. Изучение аллотропии позволяет понять особенности поведения металлов в различных условиях и использовать их свойства с максимальной эффективностью.
Основные примеры аллотропии металлов
Железо - один из самых известных металлов, также обладает аллотропией. Наиболее распространенными формами железа являются альфа-железо и гамма-железо. Альфа-железо содержит решетку типа центрированной кубической главной (CCP), а гамма-железо имеет решетку гексагонального ближайшего упаковывания (HCP). Еще одна форма железа - дельта-железо - образуется при очень высоких температурах.
Углерод - еще один пример металла, который имеет различные формы аллотропии. Наиболее известные формы углерода - алмаз и графит. Алмаз представляет собой трехмерную ковалентную сетку углерода, в то время как графит имеет слоистую структуру с атомами углерода, расположенными в виде шестиугольников. Еще одна форма углерода - фуллерены - образуются из шестиугольных колец, образующих сферы или цилиндры.
Кислород - металл со множеством аллотропных форм. Наиболее распространенной формой кислорода является диатомарный кислород, который состоит из двух атомов кислорода, связанных с двойной связью. Оксидом кислорода является также устойчивая форма кислорода, образующая одноатомные молекулы.
Железная руда - в зависимости от условий и состава, может иметь различные формы и структуры. Например, главные формы железной руды - гематит, магнетит и лимонит, и каждая из них имеет свою химическую формулу, цвет и свойства.
Это лишь некоторые из примеров аллотропии металлов. Важно понимать, что аллотропные формы металлов обладают различными свойствами и структурами, что имеет большое значение для их применения в различных областях науки и техники.
Влияние аллотропии на свойства металлов
Аллотропия, или способность металлов образовывать разнообразные структуры, имеет значительное влияние на их свойства. Различные структуры аллотропных форм металлов определяют их механические, электронные и химические характеристики.
Одним из примеров аллотропных форм является железо, которое может существовать в двух главных структурах: кубической гранецентрированной (гцк) и кубической гранецентрированной(гк). Гцк- железо обладает высокой твердостью и прочностью, а гк-железо обладает магнитными свойствами. Эти две аллотропные формы железа имеют существенно разные свойства, что позволяет использовать их в различных областях промышленности.
Некоторые металлы обладают большим разнообразием аллотропных форм. Например, углерод может существовать в виде алмаза, графита, аморфного углерода и т.д. Каждая из этих аллотропных форм углерода имеет свои уникальные свойства и пригодна для разных целей. Например, графит обладает хорошей проводимостью электричества и является материалом для изготовления электродов и лубрикантов, а алмаз обладает высокой твердостью и используется в ювелирной промышленности.
Аллотропия металлов также может влиять на их способность к образованию сплавов. Некоторые аллотропные формы металлов могут легко образовывать сплавы с другими элементами благодаря особенностям их структуры. Это позволяет создавать новые материалы с улучшенными свойствами, такими как прочность, твердость или коррозионная стойкость.
Таким образом, аллотропия металлов играет важную роль в определении их свойств и позволяет использовать их в различных областях науки и промышленности. Изучение аллотропии позволяет предсказывать и модифицировать свойства металлов, что открывает новые возможности для разработки инновационных материалов и технологий.
Структурные изменения при аллотропии

Аллотропия металлов – явление, при котором один и тот же металл может иметь разные структурные формы, называемые аллотропными модификациями. Данные модификации отличаются друг от друга своими свойствами и структурой кристаллической решетки.
Структурные изменения связаны с различными способами упаковки металлических атомов в пространстве. При аллотропии металлы могут образовывать кубическую, гексагональную или другие типы кристаллических решеток. Эти изменения структуры приводят к изменению свойств металлов, таких как плотность, твердость, электропроводность и магнитные свойства.
Примером аллотропии металлов является железо, которое в нормальных условиях имеет кубическую решетку, но при нагревании до 912 °C претерпевает структурное изменение и переходит в ферритную моноклинную фазу. Также, углерод может образовывать различные аллотропные структуры в виде алмаза, графита и аморфного углерода.
Изучение аллотропии металлов позволяет углубиться в понимание сущности материалов и их свойств. Такая информация может быть использована в разработке новых материалов с определенными свойствами и применениями в различных областях науки и промышленности.
Применение аллотропии металлов в промышленности
Аллотропия металлов, то есть их способность образовывать различные кристаллические структуры при одинаковой химической формуле, играет важную роль в промышленности. Она позволяет использовать различные аллотропные модификации металлов для получения материалов с разнообразными свойствами и применениями.
Например, железо является металлом, у которого есть несколько аллотропных модификаций, таких как аустенит, феррит и цементит. Каждая из этих модификаций обладает своими уникальными свойствами, что позволяет им использоваться в различных областях промышленности.
Аустенит, с его высокой прочностью и коррозионной стойкостью, широко применяется при производстве нержавеющей стали. Феррит, с его магнитными свойствами, используется в электротехнике и производстве соленоидов. Цементит, с его твердостью и стойкостью к износу, образует основу цемента и строительных материалов.
Кроме железа, аллотропия также играет важную роль в промышленности при производстве других металлов. Например, углерод, в зависимости от условий, может образовывать алмазы, графит или аморфный углерод. Каждая из этих модификаций имеет свои уникальные свойства и находит применение в различных отраслях, от производства алмазов до создания пишущих инструментов.
Таким образом, применение аллотропии металлов в промышленности позволяет получать материалы с различными свойствами, что важно для производства разнообразных изделий и удовлетворения потребностей различных отраслей экономики.
Исследования аллотропии металлов
Аллотропия металлов - это явление, когда разные металлы могут иметь различные кристаллические структуры и свойства. Исследование аллотропии металлов является важным направлением в материаловедении и физике металлов. Ученые из разных стран проводят эксперименты и теоретические исследования, чтобы разобраться в причинах разнообразия структур и свойств металлов.
Одним из методов исследования аллотропии металлов является рентгеноструктурный анализ. С его помощью можно определить кристаллическую структуру металла, его параметры ячейки, атомные координаты атомов и другие характеристики. Также применяются методы микроскопии, спектроскопии и термического анализа, которые позволяют изучить свойства металлов при различных условиях и установить зависимости между структурой и свойствами.
Большое внимание уделяется исследованию фазовых переходов в аллотропных системах металлов. При изменении давления и температуры металл может переходить из одной кристаллической структуры в другую, что сопровождается изменением свойств. Изучение фазовых переходов позволяет понять механизмы и условия их возникновения, а также особенности поведения металлов при экстремальных условиях.
Результаты исследований аллотропии металлов находят широкое применение в различных областях науки и техники. Они помогают разрабатывать новые материалы с улучшенными свойствами, оптимизировать производственные процессы и создавать инновационные устройства. Исследования аллотропии металлов являются важным этапом в развитии материаловедения и способствуют появлению новых технологий и материалов, которые находят применение в различных отраслях промышленности и научных исследованиях.
Вопрос-ответ

Что такое аллотропия металлов?
Аллотропия металлов - это явление, при котором один и тот же металл может образовывать различные структуры и иметь разнообразные свойства в разных физических условиях.
Почему металлы могут образовывать различные структуры?
Металлы могут образовывать различные структуры из-за особенностей их кристаллической решетки и атомной упаковки. Физические условия, такие как температура и давление, могут влиять на атомное расположение и интеракции между атомами, что приводит к изменению структуры металла.
Какие свойства могут различаться у различных структур металлов?
Различные структуры металлов могут иметь разные механические, электрические и магнитные свойства. Например, одна структура может быть хрупкой и необъемной, а другая - эластичной и прочной. Также структуры металлов могут иметь различные проводимость электричества и тепла, магнитные свойства и т.д.
Какие примеры аллотропных металлов можно привести?
Примеры аллотропных металлов включают железо, которое может образовывать структуры аустенит, бейнит и мартенсит, а также углерод, который может образовывать структуры алмаза и графита. Также аллотропия характерна для таких металлов, как олово, свинец и цирконий.
