Нитраты щелочных металлов являются солями, состоящими из аниона нитрата и положительно заряженного иона щелочного металла. Ион нитрата NO3- обладает значительной химической активностью и широко используется в различных областях, включая химическую промышленность, медицину и сельское хозяйство.
Одно из основных свойств нитратов щелочных металлов - их растворимость в воде. Это делает их удобными для использования в качестве удобрений, так как они могут легко растворяться в почве и обеспечивать доступ растениям к необходимым питательным веществам. Кроме того, нитраты щелочных металлов используются в процессе анодного окисления для производства различных продуктов, таких как джин и шампунь.
Важным свойством нитратов щелочных металлов является их способность к использованию в пиротехнике. Они способны обеспечивать яркую окраску пламени, что делает их незаменимыми компонентами при создании различных фейерверков и пиротехнических эффектов. Кроме того, нитраты щелочных металлов широко используются как стабилизаторы и окислители в процессе производства различных взрывчатых веществ.
Свойства нитратов щелочных металлов
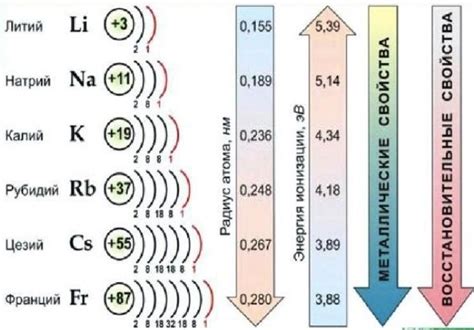
Нитраты щелочных металлов представляют собой соединения, содержащие катионы щелочных металлов (натрия, калия, лития) и анионы нитрата (NO3-). Они обычно представляют собой бесцветные кристаллы или порошки, хорошо растворимые в воде. Нитраты щелочных металлов могут быть использованы в различных областях, таких как химическая промышленность, медицина и сельское хозяйство.
Одним из основных свойств нитратов щелочных металлов является их растворимость в воде. Они легко диссоциируют в воде, образуя ионы щелочных металлов и ионы нитрата. Это делает их удобными для использования в различных процессах, таких как приготовление растворов и реакций.
Еще одним значимым свойством нитратов щелочных металлов является их окислительная активность. Ионы нитрата могут служить источником кислорода, и при взаимодействии с другими веществами они могут окислять их. Это свойство позволяет использовать нитраты для синтеза различных химических соединений и окислительных процессов.
- Нитраты щелочных металлов также обладают свойством изменять pH водных растворов. Благодаря этому, они могут использоваться в лабораторных условиях для регулирования кислотности или щелочности реакционной среды.
- Они также широко используются в сельском хозяйстве в качестве удобрений, так как они содержат азот, необходимый для роста растений. Нитраты щелочных металлов являются легко доступным источником азота, который необходим для синтеза белков и других жизненно важных органических молекул в растениях.
- Также нитраты щелочных металлов могут использоваться в медицине для лечения некоторых заболеваний, так как они могут участвовать в регулировании внутренних процессов в организме человека.
Таким образом, нитраты щелочных металлов обладают рядом полезных свойств и широко применяются в различных областях, от химической промышленности до медицины и сельского хозяйства.
Структура и состав нитратов

Нитраты щелочных металлов представляют собой соли, состоящие из катиона щелочного металла и аниона нитрата. Катионы щелочных металлов - натрия (Na+), калия (K+), лития (Li+), рубидия (Rb+) и цезия (Cs+) - обладают положительным зарядом, а анионы нитрата (NO3-) имеют отрицательный заряд.
Структура нитратных соединений включает в себя кристаллическую решетку, которая образуется благодаря взаимодействию катионов и анионов. Кристаллическая решетка может быть различной формы и структуры в зависимости от рода металла и условий образования соединения.
Состав нитратов определяется присутствием нитратного ион. Ион нитрата состоит из одного атома азота (N) и трех атомов кислорода (O). Этот ион является одним из наиболее стабильных в органической химии и обладает способностью вступать в различные химические реакции.
Важно отметить, что нитраты щелочных металлов обладают хорошей растворимостью в воде. Это свойство позволяет использовать нитраты в различных областях, таких как пищевая промышленность, медицина, сельское хозяйство и производство взрывчатых веществ.
Выводящие уравнения:
- NaNO3 (нитрат натрия) → Na+ + NO3-
- KNO3 (нитрат калия) → K+ + NO3-
- LiNO3 (нитрат лития) → Li+ + NO3-
- RbNO3 (нитрат рубидия) → Rb+ + NO3-
- CsNO3 (нитрат цезия) → Cs+ + NO3-
Таким образом, структура и состав нитратов щелочных металлов определяют их свойства и применение в различных областях человеческой деятельности.
Физические свойства нитратов

Нитраты - соли щелочных металлов и нитровой кислоты. У них есть ряд характерных физических свойств, которые определяют их поведение в различных условиях.
Первое свойство нитратов - это топотность. В сухом виде нитраты представляют собой кристаллические или аморфные вещества, которые могут быть как безводными, так и содержать одну или несколько молекул воды кристаллизации. Они обладают твердыми структурами и имеют кристаллическую решетку.
Второе свойство - это растворимость. Нитраты щелочных металлов обычно хорошо растворимы в воде, образуя прозрачные растворы. Отличительной особенностью нитратов является то, что их растворы не обладают выраженной кислотностью и не образуют осадок, кроме некоторых особенных случаев.
Третье свойство - это теплота растворения. Теплота растворения нитратов щелочных металлов зависит от конкретного соединения. Например, нитрат натрия, NaNO3, растворяется в воде с поглощением тепла, тогда как нитрат калия, KNO3, растворяется с выделением тепла. Это свойство может быть использовано в химических реакциях, например, для нагревания или охлаждения раствора.
Нитраты щелочных металлов также обладают другими свойствами, которые можно изучать, такими как плотность, плавление и другие физические характеристики. Они являются важными компонентами в различных промышленных процессах и широко используются в химической и пищевой промышленности, а также в медицине и сельском хозяйстве.
Химические свойства нитратов

Нитраты щелочных металлов - это соединения, образованные щелочными металлами и нитратной кислотой. У нитратов есть несколько характерных химических свойств.
1. Растворимость в воде. Большинство нитратов щелочных металлов хорошо растворимы в воде. Они образуют прозрачные растворы, не образуя осадка.
2. Окислительные свойства. Нитраты щелочных металлов обладают окислительными свойствами. Они могут выделять кислород и образовывать нитриты или окисленные продукты при взаимодействии с некоторыми веществами.
3. Реакция с аммиаком. Нитраты щелочных металлов образуют аммиакатные комплексы при взаимодействии с аммиаком. Это свойство используется в аналитической химии для определения содержания нитратов.
4. Эксплозивность. Некоторые нитраты щелочных металлов, включая нитрат аммония, могут быть опасными и эксплозивными в определенных условиях. Их использование взрывчатыми веществами требует особой осторожности и надлежащей обработки.
5. Реакция с металлами. Нитраты щелочных металлов могут реагировать с некоторыми металлами, образуя соответствующие нитраты. Например, реакция натрия с нитратом серебра приводит к образованию нитрата натрия и осаждению серебра.
Применение нитратов щелочных металлов

Нитраты щелочных металлов – это соединения, которые широко применяются в различных областях промышленности и научных исследований. Они обладают рядом полезных свойств, которые позволяют использовать их в разных целях.
Одним из основных применений нитратов щелочных металлов является их использование в производстве удобрений. Например, нитрат натрия (NaNO3) применяется в аграрной отрасли для подкормки почвы. Он обогащает ее азотом и способствует росту растений. Нитрат калия (KNO3) также применяется в сельском хозяйстве в качестве минерального удобрения.
Еще одно важное применение нитратов щелочных металлов – использование их в производстве взрывчатых веществ и пиротехнических смесей. Нитрат натрия и нитрат калия являются ключевыми компонентами в производстве пиротехники, такой как фейерверки и пиротехнические шоу. Они обладают высокой степенью окислительности и способны поддерживать горение и взрыв возбуждающих веществ.
Нитраты щелочных металлов также находят применение в стекольной промышленности. Они добавляются в смеси для изготовления стекла, чтобы улучшить его химическую стойкость и оптические характеристики. Кроме того, нитраты натрия и калия используются в процессе выдувания стекловолокна, придавая ему нужную структуру и прочность.
Токсичность и меры предосторожности

Нитраты щелочных металлов, такие как нитрат натрия и нитрат калия, обладают токсичными свойствами при определенных условиях. Они могут вызвать различные отрицательные эффекты на организм человека и окружающую среду.
Одним из основных источников нитратов щелочных металлов является продуктовый пищевой отход, который может попадать в почву и воду. Нитраты вымываются из почвы и могут попадать в подземные воды, что может привести к загрязнению питьевой воды.
Попадание нитратов в организм человека может привести к образованию нитрозаминов, которые являются канцерогенами и могут вызывать онкологические заболевания, такие как рак желудка и кишечника. Поэтому повышенное потребление нитратсодержащих продуктов может быть опасно для здоровья человека.
Для снижения риска токсичности нитратов щелочных металлов необходимо соблюдать некоторые меры предосторожности. Первостепенно важно ограничить потребление продуктов, богатых нитратами, таких как мясные изделия, колбасы, консервы и соленые овощи.
Также рекомендуется использовать только натуральные и свежие продукты, выращенные без применения химических удобрений. При приготовлении пищи необходимо удалять верхние слои овощей и фруктов, так как именно в них обычно содержатся наиболее высокие концентрации нитратов.
Следует также контролировать качество питьевой воды и предпочитать воду, прошедшую хорошую очистку и не содержащую высоких концентраций нитратов. При садоводстве и огородничестве необходимо применять умеренное количество удобрений, чтобы избежать избыточного накопления нитратов в почве.
Регулярный контроль содержания нитратов в продуктах и окружающей среде является неотъемлемой частью общественного здравоохранения, так как позволяет своевременно выявлять и предотвращать уровни токсичности, что способствует сохранению здоровья и экологической безопасности.
Перспективы исследований нитратов щелочных металлов
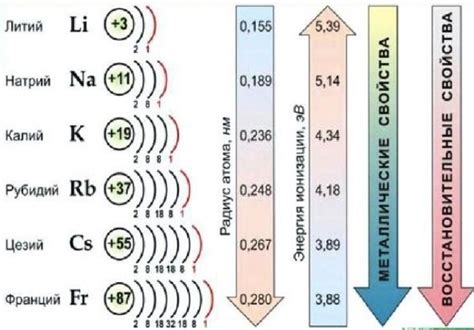
Нитраты щелочных металлов, такие как нитрат натрия (NaNO3) и нитрат калия (KNO3), широко используются в различных сферах науки и промышленности. Однако, их свойства и применение до конца еще не изучены, что открывает возможности для проведения дальнейших исследований.
Одной из перспективных областей исследований является биомедицина. Некоторые исследователи предполагают, что нитраты щелочных металлов могут быть использованы в качестве компонентов для разработки новых препаратов с антимикробными или антивирусными свойствами. Также, проведение дальнейших исследований поможет расширить наши знания о влиянии нитратов на организм человека и их влиянии на различные патологии.
Другая перспективная область исследований связана с применением нитратов щелочных металлов в энергетике. Некоторые исследования показывают, что нитраты натрия и калия могут быть использованы в качестве эффективных энергетических материалов, например, в процессе производства пиротехнических смесей или ракетных топлив.
Также, проведение исследований нитратов щелочных металлов может привести к разработке новых материалов с уникальными свойствами. Нитраты натрия и калия, например, могут быть использованы в процессе синтеза нитратных керамических материалов, которые обладают высокой термостабильностью и механической прочностью.
Для проведения исследований нитратов щелочных металлов необходима детальная характеризация их структуры и свойств. Открытие новых методов анализа и синтеза, а также изучение взаимодействия нитратов с другими веществами, представляет собой актуальную задачу для дальнейших исследований в этой области.
Вопрос-ответ

Какие свойства имеют нитраты щелочных металлов?
Нитраты щелочных металлов обладают следующими свойствами: они легко растворимы в воде, образуют прозрачные растворы, могут быть окрашены, обладают высокой термической и химической стабильностью.
Для чего используют нитраты щелочных металлов?
Нитраты щелочных металлов имеют широкое применение в разных областях. Они используются в производстве пиротехнических составов и смесей, в качестве окислителей в реакционных смесях, для приготовления нетоксичных развесных красителей, в медицине и фармацевтике, а также в аналитической химии для проведения реакций и определения различных веществ.
Какие преимущества имеют нитраты щелочных металлов перед другими соединениями?
Нитраты щелочных металлов обладают рядом преимуществ перед другими соединениями. Во-первых, они хорошо растворимы в воде, что делает их удобными в использовании. Во-вторых, они обладают высокой термической и химической стабильностью, что позволяет использовать их в различных процессах. Кроме того, они часто являются недорогими и легко доступными веществами.
