Активные металлы - группа элементов, которые характеризуются высокой химической активностью. Они легко взаимодействуют с другими веществами, выделяют большое количество энергии и обладают способностью растворяться в воде. Основными представителями активных металлов являются литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Активные металлы обладают высокой реакционной способностью из-за того, что их атомы имеют слабую связь с внешними электронными оболочками. В результате, они стремятся передать электроны другим элементам, чтобы достичь более стабильного энергетического состояния. Большинство активных металлов также обладают низкой плотностью и низкой температурой плавления.
Активные металлы имеют различные применения в разных сферах. Например, литий используется для производства легких и прочных аккумуляторов. Натрий применяется в процессе обеззараживания питьевой воды и в производстве стекла. Калий широко используется в сельском хозяйстве в качестве удобрения. Рубидий и цезий находят применение в научных исследованиях и разработке лазеров высокой мощности.
Важно помнить, что активные металлы очень реакционны и могут быть опасны при неправильном обращении с ними. Некоторые из них могут реагировать с водой или воздухом, выделяя взрывоопасные газы или огонь. Поэтому при работе с активными металлами необходимо соблюдать все меры безопасности.
В заключение, активные металлы - это элементы, которые характеризуются высокой химической активностью и способностью растворяться в воде. Они находят применение в различных отраслях, но также требуют осторожности при обращении. Изучение свойств и реакций активных металлов позволяет более глубоко понять химические процессы и использовать их потенциал в нашем повседневном и научном общении.
Активные металлы: щелочные или нет?
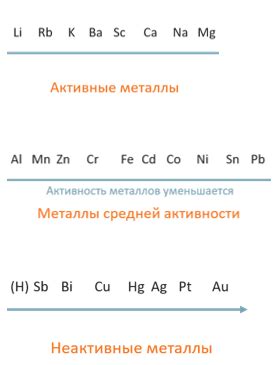
Щелочные металлы - это элементы I группы периодической системы, включающие литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают рядом характерных свойств, таких как низкая плотность, низкая температура плавления и кипения, легкость с которой они образуют ионные соединения. Одной из ключевых характеристик щелочных металлов является их реактивность - они реагируют с водой, кислородом и другими веществами.
Однако, не все активные металлы можно отнести к щелочным. Например, металлы второй группы - бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra) - не являются щелочными. Они обладают схожими свойствами с щелочными металлами, но имеют более высокую плотность и точку плавления. Кроме того, они реагируют с водой и кислородом, но не так активно, как щелочные металлы.
Некоторые активные металлы не относятся ни к щелочным, ни ко второй группе, а являются отдельной категорией. К ним относятся, например, алюминий (Al) и цинк (Zn). Они обладают большей стойкостью к окислению и имеют высокую плотность и точку плавления. Алюминий активно реагирует с кислородом, а цинк - с кислотами.
Выводы: активные металлы могут быть как щелочными (I группа периодической системы), так и не щелочными (II группа и другие металлы). Их свойства и реактивность зависят от их расположения в периодической системе.
Активные металлы - что это такое?
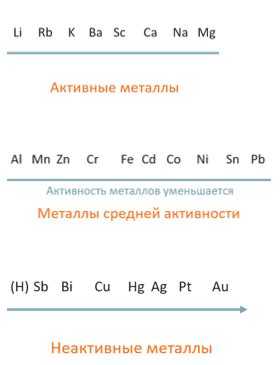
Активные металлы - это группа химических элементов, которые обладают высокой степенью активности в химических реакциях. Они проявляют способность реагировать с водой, кислотами и другими веществами, образуя соединения.
Одной из характеристик активных металлов является то, что они имеют тенденцию образовывать ионы положительного заряда. Это связано с тем, что активные металлы имеют мало электронов во внешней электронной оболочке и стремятся избавиться от них, чтобы достичь стабильной электронной конфигурации.
Как правило, активные металлы имеют металлический блеск, высокую теплопроводность и электропроводность. Они также обладают низкой плотностью и низкой температурой плавления.
Примеры активных металлов включают литий (Li), натрий (Na), калий (K), магний (Mg), алюминий (Al) и другие. Они широко используются в различных отраслях промышленности, включая производство батарей, сплавов, алюминиевых конструкций и других материалов.
Содержание активных металлов в природе
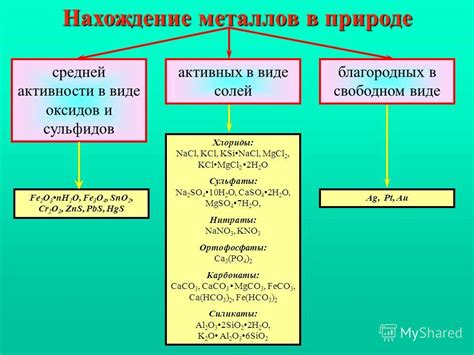
Активные металлы являются одними из наиболее распространенных элементов в природе. Они встречаются как в свободном виде, так и в соединениях с другими элементами.
Натрий (Na) – это один из наиболее известных активных металлов. Он широко распространен в морской воде, где содержится в виде хлорида натрия (NaCl). Также натрий присутствует в множестве минералов, включая фельдспаты, пироксены и микроклин.
Калий (K) – еще один распространенный активный металл. Он находится в почвах и горных породах в виде минералов, таких как калиевое полевое шпат, калиевый фельдспат и сильвинит. Калий также содержится в морской воде.
Литий (Li) – активный металл, который можно найти в различных геологических образованиях. Он присутствует в природе в виде минералов, таких как сподумен, лепидолит и пегматиты. Литий также содержится в водных растворах, включая подземные воды и геотермальные источники.
В целом, активные металлы являются важными компонентами земной коры и широко присутствуют в природе. Их содержание может значительно варьироваться в разных регионах и геологических формациях.
Щелочные металлы или нет?

Щелочные металлы – это группа элементов периодической таблицы, которые обладают высокой химической активностью и сравнительно низкой температурой плавления. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Они получили свое название из-за того, что образуют гидроксид, который обладает щелочными свойствами. Щелочные металлы являются хорошими проводниками тепла и электричества, легко реагируют с водой, образуя щелочные растворы. Их ионы обладают положительным зарядом и реагируют с отрицательно заряженными ионами, образуя стабильные соли.
Однако, не все элементы из этой группы могут быть названы "щелочными металлами". Из них только литий, натрий и калий действительно образуют щелочные растворы, а остальные – карбиды, нитриды или оксиды. Но их все равно принято относить к этой группе из-за сходных физических и химических свойств, таких как низкая плотность и низкая температура плавления.
Кратко, щелочные металлы – это группа элементов, обладающих высокой химической активностью, образующих щелочные растворы и обладающих сходными физическими и химическими свойствами. Они играют важную роль в различных отраслях науки и техники, и являются неотъемлемой частью нашей повседневной жизни.
Применение активных металлов в промышленности

Активные металлы, такие как литий, натрий и калий, имеют широкий спектр применения в промышленности.
Один из главных способов использования активных металлов – в производстве различных сплавов. Например, литий используется для создания легких, прочных и прочностных сталей, которые широко применяются в авиационной и автомобильной промышленности. Кроме того, натрий часто добавляют в алюминиевые сплавы, чтобы улучшить их прочность и устойчивость к коррозии.
Активные металлы также используются в процессе производства атомной энергии. Например, литий используется в легкомодерированных реакторах для защиты от нейтронов и стабилизации процесса деления ядерных материалов. Кроме того, калий используется в процессе обогащения урана, который является важным этапом производства ядерного топлива.
Еще одной сферой применения активных металлов является производство аккумуляторов. Например, литий-ионные аккумуляторы широко используются в мобильных телефонах, ноутбуках и электрических автомобилях благодаря своей высокой энергоемкости и низкому уровню саморазряда.
Кроме того, активные металлы применяются в химической промышленности. Например, натрий используется в процессе производства щелочи, которая является важным компонентом многих бытовых и промышленных химических продуктов. Также, натрий используется при производстве взрывчатых веществ и полимеров.
Вопрос-ответ

Какие элементы химической таблицы могут быть классифицированы как щелочные?
К щелочным металлам относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Эти элементы отличаются высокой активностью и химической реакционностью.
Каковы основные свойства щелочных металлов?
Основные свойства щелочных металлов включают низкую плотность, низкую точку плавления и кипения, мягкость, реактивность с водой и кислородом, образование щелочных оксидов и щелочных гидроксидов.
